
Wetenschap
Hoe zijn de omstandigheden van druk en temperatuur waarbij twee fasen naast elkaar bestaan in evenwicht getoond op een fasediagram?
* Fasediagram: Een fasediagram is een grafische weergave van de fysieke toestanden (vaste, vloeistof, gas) van een stof als functie van druk en temperatuur.
* Fasegrenzen: Dit zijn lijnen op het fasediagram die gebieden scheiden waar verschillende fasen stabiel zijn. Elke fasegrens vertegenwoordigt de set van druk- en temperatuuromstandigheden waarbij twee fasen naast elkaar kunnen bestaan in evenwicht.
* evenwicht: Dit betekent dat de overgangssnelheid van de ene fase naar de andere gelijk is, dus er is geen netto verandering in de hoeveelheden van elke fase.
Hier is hoe het werkt:
1. Triple Point: Het punt waar alle drie de fasen (vast, vloeibaar, gas) naast evenwicht bestaan, wordt het drievoudige punt genoemd. Dit is een specifiek punt op het fasediagram.
2. langs een fasegrens: Terwijl je langs een fasegrens beweegt, verander je de druk en temperatuur, maar de twee fasen aan weerszijden van de grens blijven in evenwicht.
3. Voorbeeld: Overweeg de grens tussen de vloeistof- en gasfasen (de dampdrukcurve). Op elk moment op deze curve kunnen de vloeistof- en gasfasen samen in evenwicht bestaan. Als u de druk verhoogt terwijl u op de curve blijft, verhoogt u de temperatuur waarbij de vloeistof en het gas naast elkaar bestaan.
Sleutelpunten:
* Elke fasegrens vertegenwoordigt een specifiek evenwicht tussen twee fasen.
* Met het fasediagram kunt u zien hoe veranderingen in druk en temperatuur de toestand van een stof beïnvloeden.
* De omstandigheden van druk en temperatuur waarbij twee fasen naast elkaar bestaan, zijn niet uniek, ze worden gedefinieerd door de fasegrens zelf.
Visualiseren het:
Stel je een fasediagram voor water voor. De vaste vloeistofgrens vertegenwoordigt het vriespunt van water bij verschillende drukken, de grens van vloeistofgas vertegenwoordigt het kookpunt en de grens van vaste gas vertegenwoordigt sublimatie. Op het drievoudige punt bestaan alle drie de fasen naast elkaar.
 Lassen met stamcellen voor chirurgische lijmen van de volgende generatie
Lassen met stamcellen voor chirurgische lijmen van de volgende generatie Moleculen bouwen zoals Tinkertoys? Een baanbrekende studie kan de weg vrijmaken
Moleculen bouwen zoals Tinkertoys? Een baanbrekende studie kan de weg vrijmaken  Over het hele spectrum:onderzoekers vinden een manier om de kleur van licht in materiaal van de volgende generatie te stabiliseren
Over het hele spectrum:onderzoekers vinden een manier om de kleur van licht in materiaal van de volgende generatie te stabiliseren Wat zijn drie redenen waarom atomen binden?
Wat zijn drie redenen waarom atomen binden?  Bacteriën onder een microscoop bekijken
Bacteriën onder een microscoop bekijken
 Soortgelijke klimaten kunnen vegetatie of landvormen worden gebruikt om de aarde in te verdelen?
Soortgelijke klimaten kunnen vegetatie of landvormen worden gebruikt om de aarde in te verdelen?  Biologen gebruiken de Aeroschup om plastic uit water te verwijderen
Biologen gebruiken de Aeroschup om plastic uit water te verwijderen Onderzoekers melden dat de door de mens waargenomen temperatuur sneller stijgt dan de werkelijke luchttemperatuur
Onderzoekers melden dat de door de mens waargenomen temperatuur sneller stijgt dan de werkelijke luchttemperatuur Een kudde flamingo's geeft hoop:zijn de zeldzame vogels voorgoed teruggekeerd naar Everglades?
Een kudde flamingo's geeft hoop:zijn de zeldzame vogels voorgoed teruggekeerd naar Everglades?  Bittere kou in januari zal het ongedierte in de veldgewassen waarschijnlijk niet verminderen
Bittere kou in januari zal het ongedierte in de veldgewassen waarschijnlijk niet verminderen
Hoofdlijnen
- Wat is een eretrocyt?
- Wat zijn de 20 takken van wetenschap en hun definities?
- Moeder-kind linkerzijde face-to-face voorkeur bleek zich uit te strekken tot walrussen en Indiase vliegende vossen
- Kunnen cellen worden getransformeerd wanneer ze zich in een competente toestand bevinden?
- Zijn er levende organismen zonder cellen?
- Identificeer de organismen die bestaan als medusa- of poliepvorm?
- Leuke wetenschappelijke experimenten op cellen
- Hoe simulatiegebaseerd leren diëtetiekstudenten voorbereidt op klinisch succes
- Hoe kan een verandering in het polypeptide de celactiviteit beïnvloeden?
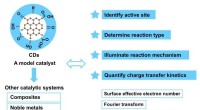
- Geavanceerde multifunctionele koolstofpunten in op foto-elektrochemie gebaseerde energieconversie
- Efficiëntiesprong bij het scheiden van para-xyleen met behulp van nieuwe koolstofmembranen

- Kleinste aardbevingen ooit gedetecteerd in metalen op micronschaal

- Nieuwe studie bevestigt de in 1953 voorspelde gegolfde eiwitstructuur

- AI-aangedreven elektronische neus om de versheid van vlees te ruiken

 Wanneer water verandert van vloeistof in gas?
Wanneer water verandert van vloeistof in gas?  Naast brandstoflucht en voldoende warmte is de andere overweging bij het creëren van een vlammende brand de?
Naast brandstoflucht en voldoende warmte is de andere overweging bij het creëren van een vlammende brand de?  Natuurlijke seismometers bevestigd op zeebodem
Natuurlijke seismometers bevestigd op zeebodem Welke planeet heeft bergen valleien vlaktes en continenten maar geen water?
Welke planeet heeft bergen valleien vlaktes en continenten maar geen water?  Is het planten van bomen om de klimaatverandering tegen te gaan 'complete onzin'?
Is het planten van bomen om de klimaatverandering tegen te gaan 'complete onzin'?  Een stap dichter bij complexe kwantumteleportatie
Een stap dichter bij complexe kwantumteleportatie Welke christenen accepteren de wetenschappelijke theorieën en waarom?
Welke christenen accepteren de wetenschappelijke theorieën en waarom?  Wat is de bron van energieconsumenten en -producenten?
Wat is de bron van energieconsumenten en -producenten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

