
Wetenschap
Waarom passen moleculen hun vormen aan in de VSEPR -theorie?
1. Elektronenparen afstoten elkaar:
* Elektronenparen, of ze nu bindende paren (gedeeld tussen atomen) of eenzame paren (niet -afgescheiden), hebben negatieve ladingen en afstoten daarom elkaar.
* Deze afstoting is elektrostatisch van aard, wat betekent dat de elektronen proberen zo ver mogelijk van elkaar weg te blijven.
2. Minimalisatie van afstoting leidt tot specifieke vormen:
* Om deze afstoting te minimaliseren, rangschikt het elektronen rond het centrale atoom zich in een specifieke geometrische opstelling.
* De geometrie die de grootste scheiding tussen elektronenparen en dus de minste afstoting bereikt, is degene die het molecuul aanneemt.
3. Verschillende soorten elektronenparen hebben verschillende afstotingssterkte:
* eenzame paren zijn weerzinwekkender dan bindingsparen. Dit komt omdat eenzame paren dichter bij de kern van het centrale atoom zijn, terwijl bindparen worden gedeeld tussen twee kernen.
* De sterkere afstoting van alleenstaande paren beïnvloedt de algehele vorm van het molecuul, waardoor bindingshoeken vaak kleiner zijn dan verwacht.
4. Moleculaire vormen voorspellen:
* VSEPR -theorie biedt een reeks regels en richtlijnen om de vorm van moleculen te voorspellen op basis van het aantal elektronenparen rond het centrale atoom.
* Het aantal binding en eenzame paren bepaalt de geometrie van de elektronenparen en de moleculaire geometrie is alleen gebaseerd op de posities van de atomen.
Voorbeeld:
* Water (H2O): Het centrale zuurstofatoom heeft twee bindingsparen en twee eenzame paren.
* geometrie van elektronenparen: Tetraëdral (vanwege vier elektronenparen)
* Moleculaire geometrie: Gebogen of v-vormig (vanwege de enige paren die de waterstofatomen dichter bij elkaar duwen)
Samenvattend passen moleculen hun vormen aan volgens de VSEPR -theorie om de afstoting tussen elektronenparen te minimaliseren, wat leidt tot specifieke geometrieën die resulteren in de meest stabiele opstelling.
 Onderzoek laat zien hoe je de symmetrie in colloïdale kristallen kunt doorbreken
Onderzoek laat zien hoe je de symmetrie in colloïdale kristallen kunt doorbreken  Welk gereedschap of gereedschap zou u gebruiken om NAD te meten de massa van een kopje zoet water en zout water vergelijken?
Welk gereedschap of gereedschap zou u gebruiken om NAD te meten de massa van een kopje zoet water en zout water vergelijken?  Wetenschappers analyseren 3D-model van eiwitten van ziekteverwekkende bacteriën
Wetenschappers analyseren 3D-model van eiwitten van ziekteverwekkende bacteriën 3 stoffen die oplossen in water?
3 stoffen die oplossen in water?  Beschrijf twee manieren waarop chemische verwering kan optreden?
Beschrijf twee manieren waarop chemische verwering kan optreden?
 UITLEG:Hoe Ida zo dodelijk 1000 mijl van aanlanding kan zijn?
UITLEG:Hoe Ida zo dodelijk 1000 mijl van aanlanding kan zijn? Vervuild meer is een arme levensader van Nicaraguanen
Vervuild meer is een arme levensader van Nicaraguanen Kan machine learning geologie onthullen die mensen niet kunnen zien?
Kan machine learning geologie onthullen die mensen niet kunnen zien? Nederlanders passen hun klimaatovertuigingen gemakkelijker aan dan hun gedrag, vinden onderzoekers
Nederlanders passen hun klimaatovertuigingen gemakkelijker aan dan hun gedrag, vinden onderzoekers  Soorten organismen die fotosynthese kunnen gebruiken
Soorten organismen die fotosynthese kunnen gebruiken
Hoofdlijnen
- Waarom gebruiken planten passief transport?
- Wat zijn 3 klassen dieetlipiden?
- Het gebruik van glowsticks in vallen verhoogt de vangst van amfibieën in studie aanzienlijk
- Welke kenmerken worden gebruikt om organismen te classificeren in domeinen en koninkrijken?
- Wat gebeurt er wanneer een nieuw organisme uit hetzelfde organisme is gevormd?
- Welke invloed heeft warmte op cellen of organismen?
- Hoe verzamelen wetenschappers gegevens?
- Hoe verschillen Paramecium dan de meeste andere protozoën?
- Nieuwe structuren bieden inzicht in hoe een bacteriële motor chemotaxis, een belangrijk infectieus proces, aandrijft
- Onderzoekers werken samen met kleine bedrijven in NM om nieuwe beademingsmaterialen te testen

- Nieuwe aanpak voor het opvangen van gas bevordert het beheer van nucleaire brandstof

- Epoxyharsen:uitharden met een druk op de knop

- Hoe ontwerp je veilige en duurzame chemicaliën
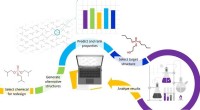
- Supermaterialen uit de magnetron

 Oproep voor kunst om Azië bij te houden
Oproep voor kunst om Azië bij te houden Satelliet ziet tropische depressie Greg als een spookachtige werveling van wolken
Satelliet ziet tropische depressie Greg als een spookachtige werveling van wolken Wat is de natuurlijke geschiedenis van de aarde gemeten?
Wat is de natuurlijke geschiedenis van de aarde gemeten?  Hoe beïnvloedt afstand de elektrische kracht tussen twee objecten?
Hoe beïnvloedt afstand de elektrische kracht tussen twee objecten?  De grens dichter bij huis brengen, één onderdompelingsreis per keer
De grens dichter bij huis brengen, één onderdompelingsreis per keer Nederlandse realityshow gaat enkele reis Mars aanbieden
Nederlandse realityshow gaat enkele reis Mars aanbieden  Waarom zijn er buffers in fermentatie?
Waarom zijn er buffers in fermentatie?
Mensen gebruiken ethanol sinds hun prehistorie in wijn, bier en andere alcoholische dranken als een recreatieve drug. Meer recentelijk is ethanol ook belangrijk geworden als alternatieve brandstof. Of het nu v
 Vlokkig grafeen maakt betrouwbare chemische sensoren
Vlokkig grafeen maakt betrouwbare chemische sensoren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

