
Wetenschap
Wat is het atoom in een watermolecuul dat meer bezocht door gedeelde elektronen?
Dit is waarom:
* elektronegativiteit: Zuurstof is elektronegatiefer dan waterstof. Elektronegativiteit is het vermogen van een atoom om elektronen aan te trekken in een chemische binding. De hogere elektronegativiteit van Oxygen betekent dat het een sterkere trek van de gedeelde elektronen in de H-O-bindingen uitoefent.
* polariteit: Deze ongelijke delen van elektronen creëert een polaire covalente binding, waarbij het zuurstofatoom een gedeeltelijke negatieve lading heeft (Δ-) en elk waterstofatoom een gedeeltelijke positieve lading (δ+) heeft.
Daarom brengen de gedeelde elektronen meer tijd dichter bij het zuurstofatoom door, waardoor het de meer bezochte atoom is.
 Wereldwijde studie van gletsjerpuin toont impact op smeltsnelheid
Wereldwijde studie van gletsjerpuin toont impact op smeltsnelheid Stappenbad-streams na natuurbrand
Stappenbad-streams na natuurbrand NASA ziet tropische cycloon koken sterk getroffen door windschering
NASA ziet tropische cycloon koken sterk getroffen door windschering Ontdekking van ontvlambaar ijs biedt aanwijzingen voor leven op andere planeten
Ontdekking van ontvlambaar ijs biedt aanwijzingen voor leven op andere planeten 80 jaar sinds de eerste berekeningen aantoonden dat de aarde opwarmde door de toenemende uitstoot van broeikasgassen
80 jaar sinds de eerste berekeningen aantoonden dat de aarde opwarmde door de toenemende uitstoot van broeikasgassen
Hoofdlijnen
- Wat is de actieve site van AB -enzym?
- Wat omringt een cel en scheidt deze van de omgeving?
- Landbouwgroepen dagen waarschuwing onkruidverdelger in Californië uit
- Wat zijn de organellen in plantencellen die energie van zonlicht veranderen in voedsel?
- Hoe slecht zijn invasieve planten voor vogels? Uit onderzoek blijkt dat grootschalige verwijdering mogelijk geen beoogde voordelen heeft
- Wat is het paren van dieren?
- Hoe poliepen van de maankwallen virale aanvallen op hun microbioom afweren
- Wat is een andere naam voor besmetting?
- Hoe worden soorten geclassificeerd?
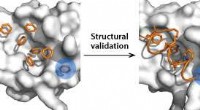
- Op benzeen gebaseerde sondes markeren twee verborgen bindingsplaatsen op een doelwit tegen kanker
- Nobelprijs voor baanbrekende manier om moleculen te bouwen die chemie groener maakten

- Mijnafval kan worden gebruikt als ingrediënt voor goedkopere productie van waterstofbrandstof

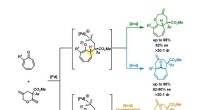
- Uiteenlopende synthese van bicyclische middelgrote ringstructuren
- Team gebruikt 3D-printen om doorstroomelektroden voor elektrochemische reactoren te optimaliseren

 Toekomstige hypersonics kunnen kunstmatig intelligent zijn
Toekomstige hypersonics kunnen kunstmatig intelligent zijn Het observeren van cellulaire activiteit, één molecuul tegelijk
Het observeren van cellulaire activiteit, één molecuul tegelijk Is kokend water voor thee een chemische of fysieke verandering?
Is kokend water voor thee een chemische of fysieke verandering?  Wie ontdekte de nucleaire envelop?
Wie ontdekte de nucleaire envelop?  Wat is gegevensorganisatie bij het oplossen van een biologisch probleem?
Wat is gegevensorganisatie bij het oplossen van een biologisch probleem?  Waarom helpt de Hubble-telescoop ons?
Waarom helpt de Hubble-telescoop ons?  Nieuw Bayesiaans kwantumalgoritme berekent direct het energieverschil van een atoom en een molecuul
Nieuw Bayesiaans kwantumalgoritme berekent direct het energieverschil van een atoom en een molecuul Sterke magnetische velden veranderen hoe wrijving in plasma werkt
Sterke magnetische velden veranderen hoe wrijving in plasma werkt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

