
Wetenschap
Hoe werkt het bicarbonaat in plasma?
bicarbonaat in plasma:een cruciale rol in de PH -regulatie van bloed
Bicarbonaationen (HCO3-) spelen een cruciale rol bij het handhaven van de pH-balans van bloedplasma, waardoor alle fysiologische processen een goed functioneren van alle fysiologische processen. Hier is hoe het werkt:
1. Buffersysteem:
* carbonzuur (H2CO3) en bicarbonaat (HCO3-) Vorm het primaire buffersysteem in bloedplasma.
* Het bicarbonaatbuffersysteem:
* neutraliseert zuren: HCO3- reageert gemakkelijk met sterke zuren (zoals melkzuur of ketonlichamen) om koolzuurzuur (H2CO3) te vormen, waardoor overtollige waterstofionen (H+) worden verwijderd en pH worden gehandhaafd.
* neutraliseert bases: H2CO3 kan H+ vrijgeven om sterke basen te neutraliseren (zoals hydroxylionen, OH-) die bijdragen aan de pH-balans.
2. Evenwicht met CO2:
* koolstofdioxide (CO2): Geproduceerd tijdens cellulaire ademhaling, diffuseert CO2 in het bloed en lost op in plasma.
* Carbonische anhydrase: Een enzym in rode bloedcellen, versnelt de omzetting van CO2 en water in carbonzuur (H2CO3).
* dissociatie: Carbonzuur dissocieert in bicarbonaationen (HCO3-) en waterstofionen (H+).
* Deze omkeerbare reactie:
* Hiermee kan het bloed CO2 van weefsels naar de longen dragen voor uitademing.
* Helpt de pH -balans te behouden door bicarbonaationen constant aan te vullen in het plasma.
3. Ademhalings- en nierregulering:
* longen: Controle CO2 -eliminatie, die de H2CO3 -niveaus en dus bicarbonaatconcentratie in het bloed beïnvloeden.
* nieren: Reguleer bicarbonaatreabsorptie en secretie, wat bijdraagt aan de homeostase van de bloed -pH.
4. Belang van bicarbonaat in de pH van het bloed:
* Normaal pH -bereik: Bloed-pH wordt gehandhaafd binnen een smal bereik van 7,35-7,45, essentieel voor de juiste enzymfunctie en cellulaire processen.
* acidose (pH <7.35): Een onbalans die leidt tot verhoogde zuurgraad, vaak als gevolg van verlaagde bicarbonaatniveaus of accumulatie van metabole zuren.
* alkalose (pH> 7.45): Een onbalans die leidt tot verhoogde alkaliteit, vaak vanwege overmatig verlies van zuur of verhoogde bicarbonaatspiegels.
Samenvattend: Bicarbonaationen fungeren als een essentieel onderdeel van het buffersysteem van het bloed, die samen met de ademhalings- en niersystemen werken om een delicate pH -balans te behouden, cruciaal voor het leven.
 Ananasboeren in Ghana hebben intensievere training nodig
Ananasboeren in Ghana hebben intensievere training nodig Teledetectie verandert de manier waarop vastgoedeconomie wordt begrepen
Teledetectie verandert de manier waarop vastgoedeconomie wordt begrepen  Groene infrastructuur biedt voordelen waar bewoners voor willen werken, studie toont
Groene infrastructuur biedt voordelen waar bewoners voor willen werken, studie toont Bladeren, stam en wortels:genetici onthullen hoe een boom weet te groeien
Bladeren, stam en wortels:genetici onthullen hoe een boom weet te groeien  Stranden verbieden zonnebrandcrème om koraalriffen te redden
Stranden verbieden zonnebrandcrème om koraalriffen te redden
Hoofdlijnen
- Wat is de medische term die niet betekent dat niet -ranselcel niet is?
- Wat is zelfrespect?
- Wat hersenetende amoeben ons kunnen vertellen over de diversiteit van het leven op aarde en de evolutionaire geschiedenis
- Bijtkrachtonderzoek onthult dinosaurus-etende kikker
- Wetenschappers gebruiken robots om te onthullen hoe roofvissen omgaan met onvoorspelbare prooien
- Heeft het zijn smaak behouden? 'Kauwgom' uit het stenen tijdperk levert menselijk DNA op
- Wat is een verband tussen koolhydraten en nucleïnezuren?
- Wat wordt geproduceerd door witte bloedcellen om pathogenen te identificeren en te neutraliseren?
- Wat presteren wetenschappers na een hypothese?
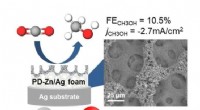
- Omzetting van kooldioxide naar methanol
- Barsten in perovskietfilms voor zonnecellen zijn gemakkelijk te genezen, studie vondsten

- Snuffelen welke plantaardige burgers het meest naar echt rundvlees ruiken

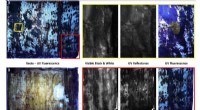
- Onderzoekers deconstrueren oud Joods perkament met behulp van meerdere beeldvormingstechnieken
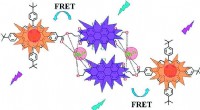
- Triplex-signaal chemosensor voor detectie met het blote oog en spectrometrische lead
 Wat is een voorbeeld van een parasitaire schimmels?
Wat is een voorbeeld van een parasitaire schimmels?  Wat gebeurt er op Jupiters Big Red Spot?
Wat gebeurt er op Jupiters Big Red Spot?  Griekse dorpen geëvacueerd vanwege bosbrand
Griekse dorpen geëvacueerd vanwege bosbrand NASA vindt tropische cycloon Wutip aan het organiseren
NASA vindt tropische cycloon Wutip aan het organiseren Onderzoekers boren diep om te begrijpen waarom de aardbeving op Sumatra zo hevig was
Onderzoekers boren diep om te begrijpen waarom de aardbeving op Sumatra zo hevig was Het maritieme grondgebied van Nieuw-Zeeland is vijftien keer zo groot als zijn landmassa:dit is waarom het land een ministerie voor de oceaan nodig heeft
Het maritieme grondgebied van Nieuw-Zeeland is vijftien keer zo groot als zijn landmassa:dit is waarom het land een ministerie voor de oceaan nodig heeft  Heeft een plantencel slechts één kern?
Heeft een plantencel slechts één kern?  Cosmeticamakers fles bacteriën voor een mooie huid
Cosmeticamakers fles bacteriën voor een mooie huid
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

