
Wetenschap
Wat is de eindtemperatuur van water als er een metaal in daalde?
* We hebben meer informatie nodig: Om de eindtemperatuur te berekenen, hebben we nodig:
* De begintemperatuur van het water: Op welke temperatuur was het water voordat het metaal werd toegevoegd?
* de massa van het water: Hoeveel water is er?
* De begintemperatuur van het metaal: Op welke temperatuur was het metaal voordat het werd gedaald?
* De massa van het metaal: Hoeveel metaal is er?
* De specifieke warmtecapaciteit van het metaal: Dit is een eigenschap van het metaal die ons vertelt hoeveel energie nodig is om zijn temperatuur met een bepaalde hoeveelheid te verhogen. Verschillende metalen hebben verschillende specifieke warmtecapaciteiten.
Het concept van warmteoverdracht
Wanneer het hete metaal in het water wordt gedropt, stroomt de warmte -energie van het heter metaal naar het koelere water. Deze stroom zal doorgaan totdat zowel het metaal als het water dezelfde temperatuur bereiken (thermisch evenwicht).
Hoe de eindtemperatuur te berekenen
Om de eindtemperatuur te berekenen, gebruiken we de volgende vergelijking:
`` `
(Massa van water * Specifieke waterwarmte * Verandering in temperatuur van water) + (Massa van metaal * Specifieke warmte van metaal * Verandering in temperatuur van metaal) =0
`` `
* Specifieke waterwarmte: Dit is een constante waarde, ongeveer 4.184 J/g ° C.
Voorbeeld
Laten we zeggen dat we hebben:
* 100 g water bij 20 ° C
* 50 g ijzer bij 100 ° C
* Specifieke ijzerwarmte is ongeveer 0,45 J/g ° C
We kunnen deze waarden aansluiten op de bovenstaande vergelijking en oplossen voor de eindtemperatuur.
Belangrijke opmerking: Deze berekening veronderstelt dat er geen warmte verloren gaat aan de omgeving. In werkelijkheid zal wat warmte altijd verloren gaan, dus de eindtemperatuur zal iets lager zijn dan wat berekend is.
 Welke kleur heeft een oplossing op het equivalentiepunt van de titratie?
Welke kleur heeft een oplossing op het equivalentiepunt van de titratie?  DNA is slechts één van de miljoenen mogelijke genetische moleculen
DNA is slechts één van de miljoenen mogelijke genetische moleculen Cool touch-shirts kunnen ervoor zorgen dat je je koel voelt op warme dagen, maar welke materialen werken het beste?
Cool touch-shirts kunnen ervoor zorgen dat je je koel voelt op warme dagen, maar welke materialen werken het beste? Herstel van DNA-schade - moleculaire inzichten
Herstel van DNA-schade - moleculaire inzichten Geef me enkele voorbeelden van pure stoffen in het dagelijks leven?
Geef me enkele voorbeelden van pure stoffen in het dagelijks leven?
 Potentiële tropische cycloon 2 in de Atlantische Oceaan onderzocht door NASA
Potentiële tropische cycloon 2 in de Atlantische Oceaan onderzocht door NASA Het verwijderen van oude structuren uit rivieren kan de vitale waterstroom herstellen
Het verwijderen van oude structuren uit rivieren kan de vitale waterstroom herstellen Is ons fosforgebruik duurzaam? De meeste belanghebbenden betwijfelen dit
Is ons fosforgebruik duurzaam? De meeste belanghebbenden betwijfelen dit  Colombia verloor bosgebied ter grootte van Sao Paulo in 2019:rapport
Colombia verloor bosgebied ter grootte van Sao Paulo in 2019:rapport Hoe kunt u uitleggen dat de concurrentie om middelen in een gebied meestal in een enkele soort intenser is dan tussen twee verschillende soorten?
Hoe kunt u uitleggen dat de concurrentie om middelen in een gebied meestal in een enkele soort intenser is dan tussen twee verschillende soorten?
Hoofdlijnen
- Wat een lijst 20 soorten wetenschap?
- Verschrikkelijke sneeuwman? Nee, onderzoek koppelt DNA-monsters van vermeende Yeti's aan Aziatische beren
- Voedingsgedrag kan een indicator zijn van voerefficiëntie bij Holstein-koeien
- Nieuwe onderzoeksaanpak:onderzoek naar het mondgevoel van voedsel met een microscoop
- Waarom hebben dierencellen het meest direct zuurstof nodig?
- Welke organismen bevatten prokaryotische cellen?
- Honden kunnen ruiken als ze gestrest zijn, suggereert onderzoek
- Wat heeft een cel?
- Volgens het principe dat bekend staat als welke genen die onafhankelijk gescheiden zijn, beïnvloeden elke erfenis niet?
- Zeer stabiele waterelektrolysekatalysator voor de productie van waterstof en zuurstof

- Door grote stille genen op te heffen, kunnen bacteriën nieuwe moleculen produceren, potentiële kandidaat-geneesmiddelen

- Metalen nanokatalysatoren imiteren de structuur van enzymen

- De grenzen van een nieuw soort chemo verkennen
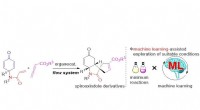
- Lastige reactiereeks krijgt een grote boost van een stroomopstelling en statistieken
 Zichtbare hydrogels voor snelle controle en controle van bloedingen
Zichtbare hydrogels voor snelle controle en controle van bloedingen Draadloze energietransmissie zou verkenning van de andere kant van de maan mogelijk kunnen maken
Draadloze energietransmissie zou verkenning van de andere kant van de maan mogelijk kunnen maken  Onderzoek wijst uit dat wifi-locatie invloed heeft op online privacygedrag
Onderzoek wijst uit dat wifi-locatie invloed heeft op online privacygedrag Een nieuw permafrostgasmysterie
Een nieuw permafrostgasmysterie Wat zijn de twee methoden voor het balanceren van chemische vergelijking?
Wat zijn de twee methoden voor het balanceren van chemische vergelijking?  Hoe bepalen astronomen de chemische samenstellingen van sterren?
Hoe bepalen astronomen de chemische samenstellingen van sterren?  Aardwetenschappers roepen op tot preventie- en waarschuwingssystemen voor overstromingen in de Himalaya
Aardwetenschappers roepen op tot preventie- en waarschuwingssystemen voor overstromingen in de Himalaya Moderne activiteiten volgen de contouren van het oude Teotihuacan
Moderne activiteiten volgen de contouren van het oude Teotihuacan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

