
Wetenschap
Wat zijn de twee methoden voor het balanceren van chemische vergelijking?
1. Trial and error (of inspectiemethode):
* proces: Deze methode omvat systematisch het aanpassen van de coëfficiënten voor elke chemische formule totdat het aantal atomen van elk element aan beide zijden van de vergelijking gelijk zijn.
* stappen:
* Begin met het meest complexe molecuul.
* Breng de atomen van één element tegelijk in evenwicht.
* Als u een polyatomisch ion tegenkomt dat aan beide zijden ongewijzigd verschijnt, behandel het dan als een enkele eenheid.
* Blijf de coëfficiënten aanpassen totdat alle elementen in evenwicht zijn.
* Voorbeeld: Balancing van de verbranding van methaan:
CH4 + O2 → CO2 + H2O
* Balans van koolstof:1 C aan elke kant
* Balans waterstof:4 uur aan elke kant, dus plaats een 2 voor H2O
* Balans zuurstof:4 O aan de productzijde, dus zet een 2 voor O2
Eindgebalanceerde vergelijking:CH4 + 2O2 → CO2 + 2H2O
2. Algebraïsche methode:
* proces: Deze methode maakt gebruik van een systeem van vergelijkingen om op te lossen voor de coëfficiënten.
* stappen:
* Wijs variabelen (a, b, c, enz.) Wijs toe aan de coëfficiënten voor elke chemische formule.
* Schrijf vergelijkingen op die de balans van elk element vertegenwoordigen.
* Los het systeem van vergelijkingen op voor de waarden van de variabelen.
* Vervang de opgeloste waarden terug in de oorspronkelijke vergelijking.
* Voorbeeld: Het balanceren van de reactie van natriumbicarbonaat met zoutzuur:
A NAHCO3 + B HCL → C NaCl + D CO2 + E H2O
* NA:A =C
* H:A + B =C + 2e
* C:a =D
* O:3a =2d + e
* CL:B =C
* Het oplossen van dit systeem geeft a =1, b =1, c =1, d =1, e =1
Eind uitgebalanceerde vergelijking:NAHCO3 + HCl → NaCl + CO2 + H2O
Welke methode moet worden gebruikt:
* Proef en fout is meestal sneller voor eenvoudige vergelijkingen.
* Algebraïsche methode is meer systematisch en nuttig voor complexe reacties.
Beide methoden bereiken hetzelfde doel:ervoor zorgen dat het aantal atomen van elk element gelijk is aan beide zijden van de chemische vergelijking, waardoor het behoud van massa in een chemische reactie wordt weergegeven.
 Nieuwe ontdekkingen en inzichten in de glasovergang
Nieuwe ontdekkingen en inzichten in de glasovergang Tweaking van legeringsmicrochemie voor vlekkeloos 3D-printen van metaal
Tweaking van legeringsmicrochemie voor vlekkeloos 3D-printen van metaal Wanneer een kopje water bij kamertemperatuur in de vriezer wordt geplaatst, zal de staatsmatter veranderen?
Wanneer een kopje water bij kamertemperatuur in de vriezer wordt geplaatst, zal de staatsmatter veranderen?  Welke chemische stof is in het grootste deel van de wereld verboden omdat de rol van de ozonlaag zijn rol heeft vernietigd?
Welke chemische stof is in het grootste deel van de wereld verboden omdat de rol van de ozonlaag zijn rol heeft vernietigd?  Waarom is koperhydroxide een zwakke base?
Waarom is koperhydroxide een zwakke base?
 Wanneer moet u varens in de tuin verplaatsen?
Wanneer moet u varens in de tuin verplaatsen?  Welke fysieke kenmerken domineren het landschap in uw gemeenschap Hoe beïnvloeden ze het leven daar?
Welke fysieke kenmerken domineren het landschap in uw gemeenschap Hoe beïnvloeden ze het leven daar?  Eco-wasmiddelen – voor groener wit in de droogkast
Eco-wasmiddelen – voor groener wit in de droogkast Een verhaal over twee valleien:de regio's Latrobe en Hunter hebben beide kolenstations, maar men heeft veel ergere kwikvervuiling
Een verhaal over twee valleien:de regio's Latrobe en Hunter hebben beide kolenstations, maar men heeft veel ergere kwikvervuiling Hoe krijgen bloemen hun voedsel?
Hoe krijgen bloemen hun voedsel?
Hoofdlijnen
- Snurken of zweven? De sterkte van het immuunsysteem van fruitvliegjes varieert
- Hoe betrouwbaar zijn schildpadden voor het meten van afval in de oceaan en de gezondheid van de zee?
- Hebben planten een celmembraan?
- Wat voor soort cel heeft geen chlorofyl of chloroplasten?
- Wat zijn de primitieve soorten kunstmatige neuron?
- Computerspellen voor vissen ontdekken waarom sommige prooien de leiding nemen en andere volgen
- Hoe vergelijkende morfologie ondersteunt de evolutietheorie?
- Wat is de studie van hoe een interne structuur van een organismen functioneert?
- Houdt mijn hond echt van mij?
- Microbieel geïnduceerde carbonaatneerslag kan grofkorrelige, zoute grond verbeteren

- Machine learning-model voorspelt fenomeen dat essentieel is voor het begrijpen van materiaaleigenschappen

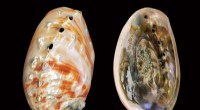
- Techniek onthult diepere inzichten in de samenstelling van parelmoer, een natuurlijk materiaal
- Kooldioxide uit schoorstenen schrobben voor schonere industriële emissies

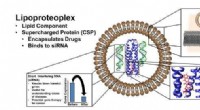
- Onderzoekers creëren biomateriaal dat zowel een krachtig medicijn als gendempers levert
 Wat is het tegenovergestelde van definitief?
Wat is het tegenovergestelde van definitief?  Nieuw papier verbindt oude tekeningen en de oorsprong van taal
Nieuw papier verbindt oude tekeningen en de oorsprong van taal Samsung, Fujitsu kiest Frankrijk voor nieuwe AI-onderzoekscentra
Samsung, Fujitsu kiest Frankrijk voor nieuwe AI-onderzoekscentra Homo erectus handbijl gevonden in Oost-Afrika
Homo erectus handbijl gevonden in Oost-Afrika Welk type straling wordt van het aardoppervlak weggereflecteerd?
Welk type straling wordt van het aardoppervlak weggereflecteerd?  Kwantumeffecten in geheugenapparaten
Kwantumeffecten in geheugenapparaten Een nieuw bioproces om plantaardig materiaal om te zetten in waardevolle chemicaliën
Een nieuw bioproces om plantaardig materiaal om te zetten in waardevolle chemicaliën Welke sensor kan in een koelkast worden gebruikt?
Welke sensor kan in een koelkast worden gebruikt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

