
Wetenschap
Welke elementen vormen geen banden met andere elementen?
* Helium (hij)
* Neon (ne)
* Argon (AR)
* Krypton (KR)
* Xenon (XE)
* Radon (RN)
Waarom vormen ze geen bindingen?
Nobele gassen hebben een volledige buitenste schaal van elektronen, wat betekent dat ze een stabiele elektronenconfiguratie hebben. Dit maakt hen zeer onuitvoerbaar en onwaarschijnlijk om elektronen te krijgen of te verliezen om chemische bindingen met andere elementen te vormen.
Uitzonderingen:
Hoewel edelgassen over het algemeen niet reactief zijn, zijn er enkele uitzonderingen:
* Xenon en Krypton: Deze zwaardere edelgassen kunnen verbindingen vormen met zeer elektronegatieve elementen zoals fluor en zuurstof onder specifieke omstandigheden.
Het is belangrijk op te merken dat de term "edelgas" niet noodzakelijkerwijs volledig inert betekent. Het betekent gewoon dat ze minder snel obligaties vormen in vergelijking met andere elementen.
 Hoeveel elektronen moeten er gewonnen worden voordat fosfor een stabiele elektronenconfiguratie heeft?
Hoeveel elektronen moeten er gewonnen worden voordat fosfor een stabiele elektronenconfiguratie heeft?  Waarom reageren aluminium en kalium wanneer ze worden gemengd?
Waarom reageren aluminium en kalium wanneer ze worden gemengd?  Hoe zouthloride af te voeren
Hoe zouthloride af te voeren
Zoutzuur, ook bekend als zoutzuur, de op water gebaseerde oplossing van waterstofchloride, is een zeer corrosief zuur. Het wordt gebruikt om batterijen en vuurwerk te maken, gelatine te maken en suiker te verwerken, maa
 Wat is de partiële stikstofdruk in lucht bij atmosferische druk (1 atm)?
Wat is de partiële stikstofdruk in lucht bij atmosferische druk (1 atm)?  Wetenschappers krijgen atomistisch beeld van afbraak van platinakatalysator
Wetenschappers krijgen atomistisch beeld van afbraak van platinakatalysator
Hoofdlijnen
- Wat is het verschil in een virusfamilie en geslacht?
- Natuurlijke selectie veroorzaakt veranderingen in populaties van organismen die niet individueel zijn, want waarom?
- Hoe introduceert meiose genetische variatie in nakomelingen?
- Wat doodt de Minnesota-eland? Onderzoekers lanceren nieuwe inspanningen om erachter te komen
- Studie lost op waarom drinken je hongerig maakt
- Wat levert ATP -levering die celactiviteiten voedt?
- Waarom restaurants willen dat je eten bestelt op je telefoon
- Hoe wordt de relatie genoemd als een bacterie zijn gastheer niet schaadt?
- Laboratoriumexperimenten met hoge resolutie laten zien hoe cellen 'eten'
- Nieuwe antivirale, antibacterieel oppervlak kan de verspreiding van infecties in ziekenhuizen verminderen

- De belofte van diepe groeven

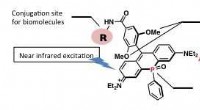
- Een nabij-infrarood fluorescerende kleurstof voor bio-imaging op lange termijn
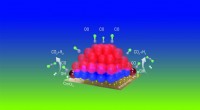
- Studie onthult de rol van platina bij de conversie van schone brandstof
- Het moleculaire canvas schilderen in superresolutie

 Nieuwe studie prijst landbouw, milieuvoordelen van biochar
Nieuwe studie prijst landbouw, milieuvoordelen van biochar Waarom zie je sterren na regendagen?
Waarom zie je sterren na regendagen?  Hoe noem je een persoon die zwaartekracht en vaccins bestudeert?
Hoe noem je een persoon die zwaartekracht en vaccins bestudeert?  Wat voor soort reactie is salpeterzuur en kaliumcarbonaat?
Wat voor soort reactie is salpeterzuur en kaliumcarbonaat?  Het gebruik van H-1B steeg enorm onder techreuzen in de Bay Area
Het gebruik van H-1B steeg enorm onder techreuzen in de Bay Area Een planeet met meer dan 16 manen?
Een planeet met meer dan 16 manen?  Back-to-the-future planten geven inzicht in klimaatverandering
Back-to-the-future planten geven inzicht in klimaatverandering Sommige kraters van de maan zijn het gevolg van interstellaire inslagen. Kunnen we vertellen welke?
Sommige kraters van de maan zijn het gevolg van interstellaire inslagen. Kunnen we vertellen welke?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

