
Wetenschap
Hoe verandert kobaltchloride met water?
De kleurverandering:
* watervrij kobaltchloride (cocl 2 ): In zijn watervrijvorm (zonder water) is kobaltchloride een blauw poeder.
* gehydrateerd kobaltchloride (cocl 2 · 6h 2 O): Bij blootstelling aan water absorbeert kobaltchloride watermoleculen en vormt een roze hydraat, cocl 2 · 6h 2 O. Deze verandering is omkeerbaar.
De chemische reactie:
De kleurverandering is te wijten aan een verandering in de coördinatieomgeving rond het kobaltion (CO
* watervrij: In de watervrijvorm wordt het kobaltion omgeven door chloride-ionen (Cl
-
), het geven van een blauwe kleur.
* gehydrateerd: Wanneer water aanwezig is, vormt het kobaltionen coördinatiebindingen met watermoleculen, ter vervanging van de chloride -ionen. De watermoleculen rond het kobaltion creëren een andere coördinatieomgeving, wat leidt tot de roze kleur.
factoren die de kleurverandering beïnvloeden:
* Waterconcentratie: Hoe meer water aanwezig is, hoe meer gehydrateerd het kobaltchloride wordt, wat leidt tot een diepere roze kleur.
* Temperatuur: De kleurverandering is meer uitgesproken bij hogere temperaturen als gevolg van verhoogde waterabsorptie.
* Vochtigheid: Kobaltchloride kan ook van kleur veranderen in vochtige omgevingen vanwege de absorptie van waterdamp uit de lucht.
Toepassingen:
Deze eigenschap kleurverandering maakt kobaltchloride nuttig in verschillende toepassingen:
* vochtindicatoren: Kobaltchloridepapier wordt gebruikt als een eenvoudige vochtindicator, die van kleur verandert van blauw naar roze in aanwezigheid van water.
* Chemische indicatoren: Het wordt gebruikt als een indicator in chemische reacties om de aanwezigheid of afwezigheid van water aan te geven.
* Desiccant (droogmiddel): Het vermogen om water te absorberen maakt het nuttig als droogmiddel in bepaalde industriële toepassingen.
Belangrijke opmerking: Kobaltchloride is een giftige chemische stof. Het moet met zorg worden behandeld en passende veiligheidsmaatregelen moeten worden genomen.
 Welk element vormt een 3 plus ion met tien elektronen?
Welk element vormt een 3 plus ion met tien elektronen?  Nieuwe digitale filterbenadering heeft tot doel chemische metingen te verbeteren
Nieuwe digitale filterbenadering heeft tot doel chemische metingen te verbeteren Wat is de chemische en structuurformule van fluorgas?
Wat is de chemische en structuurformule van fluorgas?  Hoe je spanning omzet in transformatie
Hoe je spanning omzet in transformatie  Nieuw materiaal geïnspireerd op spinnenzijde kan ons plasticprobleem helpen oplossen
Nieuw materiaal geïnspireerd op spinnenzijde kan ons plasticprobleem helpen oplossen
 NASA onderzoekt orkaandelta's vroege ochtendstructuur
NASA onderzoekt orkaandelta's vroege ochtendstructuur Aziatische karpers die in veel grotere gebieden van Lake Michigan kunnen overleven dan eerder werd gedacht
Aziatische karpers die in veel grotere gebieden van Lake Michigan kunnen overleven dan eerder werd gedacht Klimaatverandering bedreigt toekomst golf:rapport
Klimaatverandering bedreigt toekomst golf:rapport Zinkende stad:Indonesische hoofdstad op rand van ramp
Zinkende stad:Indonesische hoofdstad op rand van ramp Cyprus-studie toont grote daling van verontreinigende stoffen tijdens lockdown
Cyprus-studie toont grote daling van verontreinigende stoffen tijdens lockdown
Hoofdlijnen
- Rechts- of linkshandig? Genexpressie vertelt het verhaal van de evolutie van de slak
- Een grote stap in de richting van het verminderen van streptokokken bij op de boerderij gekweekte tilapia
- Welke chemische stof wordt soms gebruikt om cellulair plastic te maken?
- Uit nieuw onderzoek blijkt dat de tanden van walvissen nog steeds aanwezig zijn na het midden van de dracht, wat enigszins verrassend is
- Hoe een ‘evolutionaire speeltuin’ plantengenen bij elkaar brengt
- wat zijn de bestanddelen van voedsel?
- Planten worden geclassificeerd door wat in plaats van phylum?
- Wat is het belangrijkste kenmerk van gymnospermSeeds?
- Hoe fluctuerende zuurstofniveaus de evolutie van dieren kunnen hebben versneld
- Spinazie gebruikt in neutronenstudies zou het geheim kunnen ontrafelen voor een sterkere plantengroei

- Robots geactiveerd door water kunnen de volgende grens zijn

- Een SN1-reactie gebruiken om quaternaire stereocentra te maken
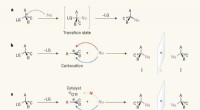
- Biochemici vangen en visualiseren een enzym wanneer het actief wordt
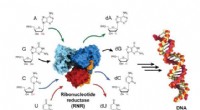
- Een sleuteldeel van de cel decoderen, atoom voor atoom

 Welk type atomen vormen doorgaans ionische of covalente bindingen?
Welk type atomen vormen doorgaans ionische of covalente bindingen?  Ferrari zegt dat de meeste van zijn auto's in 2022 hybride zullen zijn
Ferrari zegt dat de meeste van zijn auto's in 2022 hybride zullen zijn We weten niet hoeveel slachtoffers van moderne slavernij in de gevangenis zitten – waarom dat een probleem is in Groot-Brittannië
We weten niet hoeveel slachtoffers van moderne slavernij in de gevangenis zitten – waarom dat een probleem is in Groot-Brittannië  Kleine magnetische schijfjes kunnen kankercellen doden:studie
Kleine magnetische schijfjes kunnen kankercellen doden:studie Pop-up fietspaden en grassroots speeltuinen:hoe COVID-19 steden zal veranderen
Pop-up fietspaden en grassroots speeltuinen:hoe COVID-19 steden zal veranderen Woedend debat:houdt het ruimen van wolven stroperij tegen?
Woedend debat:houdt het ruimen van wolven stroperij tegen? Waarom het idee dat het Engels een gemeenschappelijke Angelsaksische oorsprong heeft, een mythe is
Waarom het idee dat het Engels een gemeenschappelijke Angelsaksische oorsprong heeft, een mythe is  Welke kracht zorgt ervoor dat een sneeuwbal die van een met gras begroeide heuvel afrolt, langzamer of sneller gaat?
Welke kracht zorgt ervoor dat een sneeuwbal die van een met gras begroeide heuvel afrolt, langzamer of sneller gaat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

