
Wetenschap
Zou u verwachten dat cesiumelement 55 min of meer reactief is dan kalium?
* Elektronenconfiguratie: Zowel cesium als kalium bevinden zich in groep 1 van de periodieke tabel (alkali -metalen). Ze hebben één valentie -elektron, dat ze gemakkelijk verliezen om een +1 kation te vormen. Cesium heeft echter een grotere atoomradius dan kalium. Dit betekent dat het valentie -elektron verder is van de kern en een zwakkere aantrekkingskracht op de kern ervaart.
* ionisatie -energie: Cesium heeft een lagere ionisatie -energie dan kalium. Dit betekent dat het minder energie vereist om zijn valentie -elektron te verwijderen, waardoor het waarschijnlijker is om te reageren en een positief ion te vormen.
* elektropositiviteit: Cesium is elektropositiever dan kalium. Dit betekent dat het een grotere neiging heeft om elektronen te verliezen en een kation te worden.
Samenvattend: De grotere atoomradius van Cesium, lagere ionisatie -energie en hogere elektropositiviteit dragen allemaal bij aan de verhoogde reactiviteit ervan in vergelijking met kalium.
 50 jaar aan gegevens van een laboratorium met een levend zuurstofminimum kunnen de toekomst van de oceanen helpen voorspellen
50 jaar aan gegevens van een laboratorium met een levend zuurstofminimum kunnen de toekomst van de oceanen helpen voorspellen Informatie over weersvoorspellingen
Informatie over weersvoorspellingen Modellen simplificeren hoe smeltende gletsjers land vervormen
Modellen simplificeren hoe smeltende gletsjers land vervormen Verontreiniging door tankstations
Verontreiniging door tankstations  Gecombineerde lokale en mondiale acties kunnen de gevolgen van veranderingen in het mariene milieu verminderen
Gecombineerde lokale en mondiale acties kunnen de gevolgen van veranderingen in het mariene milieu verminderen
Hoofdlijnen
- Is een rode bloedcel meer gespecialiseerd dan een amoeba of is het andersom uw antwoord uit te leggen?
- Wordt uw huisdier blootgesteld aan passief roken? Dit zijn de (ernstige) gezondheidsrisico’s
- Welke soort zeevruchten zijn moreel ethisch om te eten?
- Enorme golf van vlinders verlicht weerradar van Denver
- Wat zijn de orgaansystemen in het menselijk lichaam en hoe homeostase te relateren?
- Geen levend fossiel:hoe de Coelacanth onlangs tientallen nieuwe genen heeft ontwikkeld
- Waarom gebruiken wetenschappers tabel en grafiek bij het presenteren van hun gegevens of experiment?
- Waar worden de witte bloedcellen vernietigd?
- Wat betekent het als de wetenschap van het plaatsen van tings met vergelijkbare eigenschappen in groepen?
- Synthesemethode vergroot materiële mogelijkheden

- Nieuwe koolwaterstofbrandstofcellen met hoog rendement en lage kosten
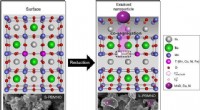
- De missie van één student om 's werelds meest waardevolle hulpbron te beschermen

- Onderzoekers ontwerpen coatings om verstopping van pijpleidingen te voorkomen

- Nieuwe aanpak maakt het gemakkelijker om nieuwe medicijnen te vinden
 Pokemon Go-maker Niantic maakt een spel van de wereld
Pokemon Go-maker Niantic maakt een spel van de wereld Sprint lanceert mobiel 5G-netwerk in Atlanta, Dallas-Fort Worth, Houston en Kansas City
Sprint lanceert mobiel 5G-netwerk in Atlanta, Dallas-Fort Worth, Houston en Kansas City Voor mensen die stotteren, het gemak van spraakassistenttechnologie blijft buiten bereik
Voor mensen die stotteren, het gemak van spraakassistenttechnologie blijft buiten bereik Wat zijn geen voorbeelden van colloïden?
Wat zijn geen voorbeelden van colloïden?  Hoe wordt energie omgezet in de valtoren?
Hoe wordt energie omgezet in de valtoren?  Biosensortechnologieën om effectievere benaderingen van ziektebehandeling te bieden
Biosensortechnologieën om effectievere benaderingen van ziektebehandeling te bieden Duitsers zijn voorstander van een snelle stopzetting van het gebruik van steenkool naarmate het besluit nadert
Duitsers zijn voorstander van een snelle stopzetting van het gebruik van steenkool naarmate het besluit nadert Hoe werkt een naverbrander?
Hoe werkt een naverbrander?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

