
Wetenschap
Wat is de theoretische opbrengst van aluminium die kan worden geproduceerd door reactie van 60,0 g oxide met 30,0 koolstof volgens de volgende chemische AL2O3 3C 2AL 3CO?
1. Evenwichtige chemische vergelijking:
De evenwichtige chemische vergelijking is al voorzien:
Al₂o₃ + 3c → 2al + 3co
2. Bereken mol reactanten:
* mol al₂o₃:
- Molaire massa van al₂o₃ =(2 * 26,98 g/mol) + (3 * 16,00 g/mol) =101,96 g/mol
- mol al₂o₃ =(60,0 g) / (101,96 g / mol) =0,588 mol
* mol C:
- Molaire massa van C =12,01 g/mol
- mol c =(30,0 g) / (12,01 g / mol) =2,498 mol
3. Bepaal de beperkende reactant:
* Vergelijk de molverhoudingen: De gebalanceerde vergelijking laat zien dat 1 mol al₂o₃ reageert met 3 mol C.
* Bereken de vereiste mol C: 0,588 mol al₂o₃ * (3 mol c / 1 mol al₂o₃) =1.764 mol c
* Conclusie: We hebben meer mol C (2.498 mol) dan nodig (1.764 mol) voor de reactie. Daarom is Al₂o₃ de beperkende reactant.
4. Bereken theoretische opbrengst van aluminium:
* molverhouding: Uit de evenwichtige vergelijking produceert 1 mol al₂o₃ 2 mol al.
* mol al: 0,588 mol al₂o₃ * (2 mol AL / 1 mol al₂o₃) =1.176 mol Al
* Mass van Al: 1.176 Mol Al * (26,98 g/mol) = 31,7 g AL
Daarom is de theoretische opbrengst van aluminium die kan worden geproduceerd 31,7 g.
 Nieuwe technologie maakt snelle eiwitsynthese mogelijk
Nieuwe technologie maakt snelle eiwitsynthese mogelijk Wat is de rol van biosfeer bij het vormen van atmosferische zuurstof op het huidige niveau?
Wat is de rol van biosfeer bij het vormen van atmosferische zuurstof op het huidige niveau?  Onderzoek geeft eindelijk antwoord waarvoor dolken uit de bronstijd werden gebruikt
Onderzoek geeft eindelijk antwoord waarvoor dolken uit de bronstijd werden gebruikt  Poreuze polymeerfilms met vormgeheugen
Poreuze polymeerfilms met vormgeheugen Wat is de betekenis van de ionisatietoestand bij het bepalen van de chemische eigenschappen van een stof?
Wat is de betekenis van de ionisatietoestand bij het bepalen van de chemische eigenschappen van een stof?
 Hoge hitte maar geen record:2018 was het 4e warmste jaar op aarde
Hoge hitte maar geen record:2018 was het 4e warmste jaar op aarde Sociale media gebruiken om klimaatverandering aan te pakken
Sociale media gebruiken om klimaatverandering aan te pakken Expert:Geen enkele, one-size-fits-all oplossing voor het probleem van plastic afval
Expert:Geen enkele, one-size-fits-all oplossing voor het probleem van plastic afval Diepzeekoralen onthullen geheimen van snelle toename van koolstofdioxide naarmate de laatste ijstijd eindigde
Diepzeekoralen onthullen geheimen van snelle toename van koolstofdioxide naarmate de laatste ijstijd eindigde Studie:Uitbreiding van telewerken zou vervuiling tot 10% verminderen
Studie:Uitbreiding van telewerken zou vervuiling tot 10% verminderen
Hoofdlijnen
- Zoogdiercellen observeren met supersnelle zachte röntgenstralen
- Wat is de beschermende barrière die alle cellen omsluit?
- Waar wordt de kern in de cel gevonden en waarom?
- Doorbraak in het begrijpen hoe dodelijke pneumokokken de immuunafweer vermijden
- Centriole: definitie, functie en structuur
- Microscopische veerkenmerken onthullen de kleuren van fossiele vogels en verklaren waarom kasuarissen schitteren
- Uit onderzoek blijkt dat klimaatverandering tropische vissen helpt het Australische oceaanwater binnen te dringen
- Wat zijn slijmvliezen?
- De wetenschap van hoe planten trauma registreren omvat een voorloper van de calciumgolf
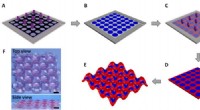
- Hydrogels met periodiek patroon:een model voor coöperatieve vervorming
- Smart label kan je op een dag laten weten wanneer je voedsel en cosmetica moet weggooien

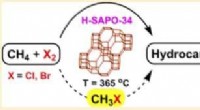
- De voetafdruk verkleinen van een broeikasgas dat krachtiger is dan koolstofdioxide
- Onderzoekers beschrijven structuren, mechanismen die bacteriën in staat stellen antibiotica te weerstaan

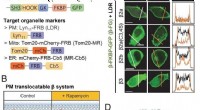
- Nieuwe studie onthult de interactie van calciumkanalen
 Wat is de functie van recirculatie in de elektriciteitscentrale?
Wat is de functie van recirculatie in de elektriciteitscentrale?  Is de ozonlaag op weg naar herstel?
Is de ozonlaag op weg naar herstel?  Hoe beantwoord je Apunnet Square -vraag?
Hoe beantwoord je Apunnet Square -vraag?  Bevat koolstof vier ionische bindingen in zijn verbindingen?
Bevat koolstof vier ionische bindingen in zijn verbindingen?  Azijn en zout gebruiken om een cent te laten verdwijnen
Azijn en zout gebruiken om een cent te laten verdwijnen ongeveer 1, 000 geëvacueerd terwijl Canadese branden de stad overspoelen
ongeveer 1, 000 geëvacueerd terwijl Canadese branden de stad overspoelen De ontdekking van fantoomvulkanen geeft nieuwe hoop aan voor olie- en gasexploratie in de Noordzee
De ontdekking van fantoomvulkanen geeft nieuwe hoop aan voor olie- en gasexploratie in de Noordzee Reageert zwavel op zonlicht?
Reageert zwavel op zonlicht?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

