
Wetenschap
Wat is een juiste beschrijving van de enthalpie -reactie?
Reaction van reactie:een correcte beschrijving
De enthalpie van de reactie, vaak gesymboliseerd als ΔH, verwijst naar de verandering in enthalpie Dat gebeurt tijdens een chemische reactie. Het vertegenwoordigt de warmte -energie geabsorbeerd of vrijgegeven tijdens de reactie onder constante druk.
Hier is een meer gedetailleerde uitsplitsing:
* Enthalpy (H): Dit is een thermodynamische eigenschap die de totale energie van een systeem vertegenwoordigt, inclusief de interne energie en het product van zijn druk en volume.
* Verandering in enthalpie (ΔH): Het is het verschil in enthalpie tussen de producten en reactanten van een reactie.
* exotherme reacties: Deze reacties Verslaat warmte in de omgeving, wat resulteert in een negatieve AH -waarde.
* Endotherme reacties: Deze reacties absorberen warmte Uit de omgeving, resulterend in een positieve AH -waarde.
Sleutelpunten:
* De enthalpie van reactie is een toestandsfunctie , wat betekent dat het alleen afhangt van de initiële en uiteindelijke toestanden van het systeem, niet op het pad dat wordt genomen om ze te bereiken.
* Het wordt meestal uitgedrukt in joules (j) of kilojoules (kj) .
* De enthalpie van reactie is een nuttig hulpmiddel voor het voorspellen van de warmtestroom geassocieerd met een reactie en het bepalen van de haalbaarheid ervan.
Samenvattend kwantificeert de reactie van de reactie de warmte -energie die is uitgewisseld tussen een chemische reactie en zijn omgeving.
Hoofdlijnen
- Hoe origami ziektediagnoses kan bepalen
- Is een bron van genetische variatie waarbij de ruilende secties chromosomen tijdens meiose betrokken zijn?
- Onderzoekers ontdekken hoe zenuwcellen in de hersenen van vleermuizen reageren op hun omgeving en sociale interacties met andere vleermuizen
- Lamarck stelde een foutief evolutionair mechanisme voor dat tegenwoordig bekend staat als?
- Wat zijn de kenmerken van een tuinwt?
- Wat vormt een selectief permeabel membraan?
- Wat is microtoxine?
- Kopiëren of innoveren? Studie werpt licht op de chimpanseecultuur
- Wat is het ruwe endoplasmatisch reticulum?
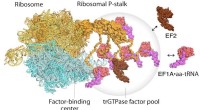
- High-speed atomic force microscopie visualiseert celeiwitfabrieken
- Onderzoekers maken waterstofbrandstof uit zeewater

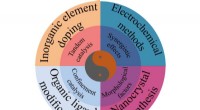
- Afstemmingsstrategieën en structuureffecten van elektrokatalysatoren voor de koolstofdioxidereductiereactie
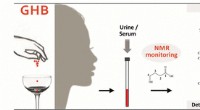
- De detectie van een date rape drug verbeteren
- Ingenieurs onthullen moleculaire geheimen van de krachten van koppotigen

 3 kenmerken van mengsel uit pure substantie?
3 kenmerken van mengsel uit pure substantie?  1,5 kilogram is gelijk aan hoeveel gram?
1,5 kilogram is gelijk aan hoeveel gram?  Zeevogelnesten zitten vol met weggegooid plastic afval
Zeevogelnesten zitten vol met weggegooid plastic afval Smoggiere luchten, lagere scores? Een Braziliaans onderzoek onderzoekt de effecten van luchtvervuiling op de cognitieve prestaties van leerlingen
Smoggiere luchten, lagere scores? Een Braziliaans onderzoek onderzoekt de effecten van luchtvervuiling op de cognitieve prestaties van leerlingen  Hoe een Seismograph
Hoe een Seismograph Indringende vraag:Wat is burgerjournalistiek?
Indringende vraag:Wat is burgerjournalistiek?  Welke mineralen zijn in Iowa?
Welke mineralen zijn in Iowa?  Bestaat al het leven uit materie?
Bestaat al het leven uit materie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


