
Wetenschap
Wat is de kracht die watermoleculen aan elkaar verbindt?
Hier is een uitsplitsing:
* polariteit: Watermoleculen zijn polair, wat betekent dat ze een enigszins positief uiteinde hebben (nabij de waterstofatomen) en een enigszins negatief uiteinde (nabij het zuurstofatoom). Dit gebeurt omdat zuurstof elektronegatiefer is dan waterstof, waardoor de gedeelde elektronen dichter bij zichzelf worden getrokken.
* Attractie: Het positieve uiteinde van het ene watermolecuul wordt aangetrokken door het negatieve uiteinde van een ander watermolecuul. Deze aantrekkingskracht wordt een waterstofbinding genoemd.
* Kracht: Waterstofbindingen zijn relatief zwak in vergelijking met covalente bindingen, maar ze zijn nog steeds belangrijk omdat ze watermoleculen bij elkaar houden, waardoor water zijn unieke eigenschappen krijgt.
Eigenschappen van water die te wijten zijn aan waterstofbinding:
* Hoog kookpunt: Water heeft een hoger kookpunt dan verwacht vanwege zijn molecuulgewicht vanwege de energie die nodig is om de waterstofbruggen te verbreken.
* Hoge oppervlaktespanning: Watermoleculen aan het oppervlak worden sterker aangetrokken tot elkaar dan tot de lucht, waardoor een sterke oppervlaktespanning ontstaat.
* Universeel oplosmiddel: Met de polariteit van het water kan het veel stoffen oplossen, waardoor het een goed oplosmiddel is.
Samenvattend is waterstofbinding de kracht die watermoleculen bij elkaar houden en water zijn unieke eigenschappen geeft.
 Doorbraak naar het oplossen van het structurele mysterie van glas
Doorbraak naar het oplossen van het structurele mysterie van glas Synthesestudies transformeren afvalsuiker voor toepassingen voor duurzame energieopslag
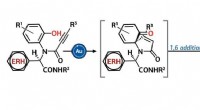
Synthesestudies transformeren afvalsuiker voor toepassingen voor duurzame energieopslag Een moleculaire motor gebruiken om de voorkeur van anionbindende katalysatoren te veranderen
Een moleculaire motor gebruiken om de voorkeur van anionbindende katalysatoren te veranderen Gericht op het industriële gebruik van kleikolomchromatografie voor optische resolutie
Gericht op het industriële gebruik van kleikolomchromatografie voor optische resolutie  Waarom dacht Thomson dat een atoom positieve ladingen moest bevatten?
Waarom dacht Thomson dat een atoom positieve ladingen moest bevatten?
 Indiase reddingswerkers jagen op overlevenden terwijl de moessontol 115 . bereikt
Indiase reddingswerkers jagen op overlevenden terwijl de moessontol 115 . bereikt Is het verbranden van afval een goede manier om ermee om te gaan? Afvalverbranding in 5 grafieken
Is het verbranden van afval een goede manier om ermee om te gaan? Afvalverbranding in 5 grafieken Klimaatcyclus La Nina kan in 2021 weer opduiken:UN
Klimaatcyclus La Nina kan in 2021 weer opduiken:UN Studie identificeert het belang van atmosferische rivieren voor Nieuw-Zeeland
Studie identificeert het belang van atmosferische rivieren voor Nieuw-Zeeland Klimaatexperts publiceren de nieuwste wetenschap over projecties van zeespiegelstijging
Klimaatexperts publiceren de nieuwste wetenschap over projecties van zeespiegelstijging
Hoofdlijnen
- Wil je tijgers redden? Je kunt maar beter je cijfers op een rij hebben
- Biologen ontdekken hoe planten stamcellen reconstrueren
- Onderzoekers laten zien hoe spoorwegwormen rood licht produceren
- Nu weten we waarom wortels oranje zijn
- Lamarck stelde een foutief evolutionair mechanisme voor dat tegenwoordig bekend staat als?
- Welke structuur in het urinestelsel is het belangrijkst?
- Nobel werpt licht op paleogenetica, studie van oud DNA
- Hoe hebben wetenschappers ontdekt dat genen zijn gemaakt van DNA?
- Wat is structuur?
- Titaandioxide-sterren in onderzoek bij synchrotron in Krakau

- Chemicus ontwikkelt synthesemethode voor 28 biologisch actieve moleculen
- Wetenschappers zoeken naar nieuwe benaderingen om geregenereerd uranium te verrijken

- Forensisch onderzoek van FBI bereikt snelheid in Hollywood, onderzoeker zegt:

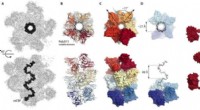
- Wetenschappers maken beelden van antilichamen die samenwerken tegen malaria
 Amerikaanse en Iraanse onderzoekers werken samen aan herstel van het Urmia-meer
Amerikaanse en Iraanse onderzoekers werken samen aan herstel van het Urmia-meer Mediterrane regenval onmiddellijk beïnvloed door veranderingen in broeikasgassen
Mediterrane regenval onmiddellijk beïnvloed door veranderingen in broeikasgassen Sedimenten in meren tonen verband tussen klimaatverandering en bosbranden in Aussie Alpen
Sedimenten in meren tonen verband tussen klimaatverandering en bosbranden in Aussie Alpen Een halve graad minder opwarming kan extreme neerslag voorkomen
Een halve graad minder opwarming kan extreme neerslag voorkomen Wat is een subtropische storm en hoe verschilt deze van een tropisch of extratropisch systeem?
Wat is een subtropische storm en hoe verschilt deze van een tropisch of extratropisch systeem?  Onderzoekers ontwikkelen nieuw platform om elektronische apparaten van de volgende generatie geavanceerder te maken
Onderzoekers ontwikkelen nieuw platform om elektronische apparaten van de volgende generatie geavanceerder te maken Proba-V beelden Portugese bosbrand
Proba-V beelden Portugese bosbrand Lijst met unieke planten voor loofbossen
Lijst met unieke planten voor loofbossen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

