
Wetenschap
Waarom worden elektronen meestal gevonden in de buurt van de kern?
* Tegengestelde ladingen trekken aan: De kern van een atoom bevat protonen, die positief geladen zijn. Elektronen daarentegen hebben een negatieve lading.
* Sterke kracht: Dit verschil in lading creëert een sterke elektrostatische kracht die de negatief geladen elektronen naar de positief geladen kern trekt.
* energieniveaus: Elektronen rondom de kern rond de kern. Ze bestaan in specifieke energieniveaus of schelpen. Hoe lager het energieniveau, hoe dichter het elektron bij de kern is. Elektronen hebben de neiging om de laagste beschikbare energieniveaus te bezetten, die dichter bij de kern liggen.
* kwantummechanica: Kwantummechanica beschrijft het gedrag van elektronen in atomen nauwkeuriger dan de klassieke fysica. Het legt uit hoe elektronen bestaan in wolken van waarschijnlijkheid, bekend als orbitalen, rond de kern. Hoewel de exacte locatie van een elektron niet kan worden voorspeld, is de kans om dichter bij de kern te zijn hoger.
Samenvattend: De aantrekkelijke kracht tussen de negatief geladen elektronen en de positief geladen kern, samen met de neiging van elektronen om lagere energieniveaus te bezetten, houdt elektronen gebonden aan het atoom en dicht bij de kern.
 De dampdruk van zuiver water is 30 mm van de 10 glucose-oplossing?
De dampdruk van zuiver water is 30 mm van de 10 glucose-oplossing?  Waarom verandert een vaste stof in vloeistof wanneer warmte wordt toegevoegd?
Waarom verandert een vaste stof in vloeistof wanneer warmte wordt toegevoegd?  Waarom wordt de waterige oplossing van calciumhydroxide vervaagd wanneer u koolstofdioxide erin stuurt?
Waarom wordt de waterige oplossing van calciumhydroxide vervaagd wanneer u koolstofdioxide erin stuurt?  Antwoord op bacteriële antibioticaresistentie kan worden gevonden in planten
Antwoord op bacteriële antibioticaresistentie kan worden gevonden in planten Hoe balanceer je de chemische vergelijking van 3Na plus AlCl3 - 3NaCl Al?
Hoe balanceer je de chemische vergelijking van 3Na plus AlCl3 - 3NaCl Al?
Hoofdlijnen
- Onderzoekers laten zien hoe het ontwerp van gebouwen de bacteriën binnenshuis beïnvloedt
- DNA-onderzoekers roepen botverzamelaars op om toegang tot botten te delen
- Wat is de definitie van hersenstam en cerebellum?
- De verschillen tussen mitochondriën en chloroplasten in structuur
- Begrijpen wat de harten van gevangen gorilla's doet tikken
- Wat is een term voor decomposer?
- Hoe inktviscamouflage huidkanker bij mensen kan helpen voorkomen
- Lijst met schimmelvoordelen
- Hoe vindt een mug menselijk lichaam?
- Nieuwe composietmaterialen verlengen de levensduur van reserveonderdelen voor apparatuur en voertuigen

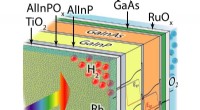
- Nieuw wereldrecord voor directe zonne-watersplitsingsefficiëntie
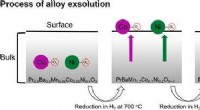
- Hoogwaardige zelf-geassembleerde katalysator voor SOFC
- Nieuwe techniek kan gevangen koolstof waardevoller maken

- Kathodedefecten verbeteren de batterijprestaties

 Milieuproblemen veroorzaakt door raketvluchten boven San Diego County
Milieuproblemen veroorzaakt door raketvluchten boven San Diego County  Wat is de elektriciteit die wordt geproduceerd bij het opwekken?
Wat is de elektriciteit die wordt geproduceerd bij het opwekken?  Hoe doodt hitte? Het brengt je hersenen in verwarring. sluit organen af. overwerkt het hart.
Hoe doodt hitte? Het brengt je hersenen in verwarring. sluit organen af. overwerkt het hart.  Wat is het verschil tussen oude en echte bacteriën?
Wat is het verschil tussen oude en echte bacteriën?  Algen:vijverschuim of voedsel van de toekomst?
Algen:vijverschuim of voedsel van de toekomst?  China's waterkracht-razernij verdrinkt heilige bergen
China's waterkracht-razernij verdrinkt heilige bergen Het ontsluiten van de belofte van benaderend computergebruik voor AI-versnelling op de chip
Het ontsluiten van de belofte van benaderend computergebruik voor AI-versnelling op de chip Hoe spoor je een geheimzinnige havik op? Volg de isotopen
Hoe spoor je een geheimzinnige havik op? Volg de isotopen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

