
Wetenschap
Waarom wordt de waterige oplossing van calciumhydroxide vervaagd wanneer u koolstofdioxide erin stuurt?
1. Calciumhydroxide (limwater):
* Calciumhydroxide is een zwakke basis en de waterige oplossing staat bekend als limwater.
* Limwater is duidelijk en kleurloos.
2. Reactie met koolstofdioxide:
* Wanneer koolstofdioxidegas door limwater wordt geborreld, reageert het met het calciumhydroxide om calciumcarbonaat (caco₃) en water (H₂O) te vormen.
* De chemische vergelijking voor deze reactie is:
`` `
CA (OH) ₂ (aq) + co₂ (g) → caco₃ (s) + h₂o (l)
`` `
3. Vorming van het neerslag:
* Calciumcarbonaat (caco₃) is een onoplosbare witte vaste stof. Dit betekent dat het niet goed oplost in water.
* Naarmate de reactie vordert, trekt het onoplosbare calciumcarbonaat uit de oplossing en vormt een melkwitte suspensie.
4. Wazig uiterlijk:
* De suspensie van kleine calciumcarbonaatdeeltjes verspreidt licht in alle richtingen, waardoor de oplossing bewolkt of wazig lijkt.
Samenvattend:
Het koolstofdioxide reageert met het calciumhydroxide en produceert een wit neerslag van calciumcarbonaat. Dit neerslag maakt de oplossing bewolkt en ondoorzichtig, wat leidt tot het wazige uiterlijk.
 Dual-ligand-strategie helpt bij het bereiken van perfecte asymmetrische polymerisatie met kinetische resolutie
Dual-ligand-strategie helpt bij het bereiken van perfecte asymmetrische polymerisatie met kinetische resolutie  De atomaire massa berekenen van een element dat een isotopen van een mengsel bevat?
De atomaire massa berekenen van een element dat een isotopen van een mengsel bevat?  Wetenschappers vinden schadelijke chemicaliën in huishoudstof
Wetenschappers vinden schadelijke chemicaliën in huishoudstof Is covalente binding oplosbaar in water?
Is covalente binding oplosbaar in water?  Een metallopeptide richt zich op en verstoort de mitochondriale functie in stamcellen van borstkanker
Een metallopeptide richt zich op en verstoort de mitochondriale functie in stamcellen van borstkanker
 Wazige luchten, slechte luchtkwaliteit:verergert de havencongestie de vervuiling van LA?
Wazige luchten, slechte luchtkwaliteit:verergert de havencongestie de vervuiling van LA? Hernieuwbare energiebronnen kunnen de klimaatdoelen van Parijs niet halen:studie
Hernieuwbare energiebronnen kunnen de klimaatdoelen van Parijs niet halen:studie Waarom is landbouw in bergachtige gebieden zo moeilijk zonder terrassen?
Waarom is landbouw in bergachtige gebieden zo moeilijk zonder terrassen?  Hittegolven op de oceaan en zwakkere wind zullen Australië nog een tijdje warm houden
Hittegolven op de oceaan en zwakkere wind zullen Australië nog een tijdje warm houden Het ontmaskeren van de bevolkingsbom
Het ontmaskeren van de bevolkingsbom
Hoofdlijnen
- Roept op tot regelgevende maatregelen om de openbaarmaking van biodiversiteit te versterken
- Wat zijn enkele veel voorkomende toepassingen van gist?
- Wat is een proces door welke cellen in structuur veranderen?
- Hoe verschillen oogenese en spermantogenese?
- Hoe verschijnen cellen wanneer Brownse beweging hun beweging veroorzaakt?
- Nieuwe studie werpt licht op hoe intracellulaire pathogenen het immuunsysteem activeren
- Tot de kern komen van hoe cowpea groeit in moeilijke omstandigheden
- Welke gespecialiseerde structuur zou je verwachten in een cel die is aangepast om energie te produceren?
- Is koolstofdioxide of de groei van het micro -organisme een karakteristiek leven?
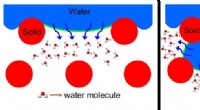
- Wetenschappers onthullen belangrijke inzichten in opkomende waterzuiveringstechnologie
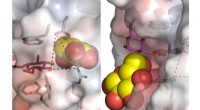
- Het blootleggen van ultrasnelle dynamiek van plantenenzymen kan de graanproductie, de medische en farmaceutische industrie vooruit helpen
- In Australië worden zelfsteriliserende micronaalden ontwikkeld voor veiligere vaccinaties
- Nieuwe zwaailampen verlichten het interieur
- Ultradun, gasdichte coatings voor PET-flessen

 Wat is het mechanische chemische of nucleaire mechanische water?
Wat is het mechanische chemische of nucleaire mechanische water?  Het probleem van in massa geproduceerde moleculaire knooppunten kraken
Het probleem van in massa geproduceerde moleculaire knooppunten kraken Vraag en antwoord:EPA voltooit het uitfaseringsplan voor forever-chemicaliën bekend als PFAS
Vraag en antwoord:EPA voltooit het uitfaseringsplan voor forever-chemicaliën bekend als PFAS  Natuurkundigen maken transparante geleiders door middel van stempelen en groeien
Natuurkundigen maken transparante geleiders door middel van stempelen en groeien Efficiënte opname van uranium(VI) gerealiseerd door gelaagd mangaanthiofosfiet geïntercaleerd met ammonium
Efficiënte opname van uranium(VI) gerealiseerd door gelaagd mangaanthiofosfiet geïntercaleerd met ammonium Welke factoren beïnvloeden het smeltpunt?
Welke factoren beïnvloeden het smeltpunt?  Wetenschappers laten zien hoe vloeibare brandstoffen in polymere gels kunnen worden opgeslagen om explosies en branden te voorkomen
Wetenschappers laten zien hoe vloeibare brandstoffen in polymere gels kunnen worden opgeslagen om explosies en branden te voorkomen Amerikaanse westkust:in frontlinie van nucleaire wolk?
Amerikaanse westkust:in frontlinie van nucleaire wolk?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

