
Wetenschap
Waarom verandert een vaste stof in vloeistof wanneer warmte wordt toegevoegd?
1. Moleculaire structuur:
* vaste stoffen: Moleculen in een vaste stof zijn strak gepakt in een vaste, geordende opstelling. Ze hebben sterke intermoleculaire krachten die ze op hun plaats houden.
* vloeistoffen: Moleculen in een vloeistof zijn losjes verpakt en kunnen zich om elkaar heen bewegen. Ze hebben zwakkere intermoleculaire krachten dan vaste stoffen.
2. De rol van warmte:
* Warmte -energie: Wanneer warmte wordt toegevoegd aan een vaste stof, verhoogt dit de kinetische energie (energie van beweging) van de moleculen. De moleculen trillen sneller.
* Breaking Bonds: Naarmate de moleculen krachtiger trillen, worden de intermoleculaire krachten die ze in een vaste structuur houden verzwakken. Uiteindelijk worden de trillingen sterk genoeg om de bindingen te overwinnen, waardoor de moleculen loskomen van hun vaste posities.
* overgang: Deze overgang van een vaste, geordende regeling naar een meer mobiele, minder geordende status is wat de verandering van vaste naar vloeistof definieert.
3. Smeltpunt:
* specifieke temperatuur: Elke stof heeft een specifiek smeltpunt, de temperatuur waarbij hij overgaat van vaste naar vloeistof. Dit punt wordt bepaald door de sterkte van de intermoleculaire krachten in de stof.
* constante temperatuur: Tijdens het smeltproces blijft de temperatuur constant, hoewel er warmte wordt toegevoegd. Dit komt omdat de energie wordt gebruikt om de bindingen te verbreken, niet om de temperatuur te verhogen.
Kortom:
Het toevoegen van warmte biedt energie aan de moleculen in een vaste stof. Deze verhoogde energie verzwakt de bindingen die ze bij elkaar houden, waardoor ze vrijer kunnen bewegen en overgaan in een vloeibare toestand.
 Hoeveel elektronen bevinden zich in de buitenste ring van cesium?
Hoeveel elektronen bevinden zich in de buitenste ring van cesium?  In welke anorganische verbinding treden de meeste reacties op chemicaliën op?
In welke anorganische verbinding treden de meeste reacties op chemicaliën op?  Onderzoekers lossen controverse op over energiekloof van Van der Waals-materiaal
Onderzoekers lossen controverse op over energiekloof van Van der Waals-materiaal Pervaporatiemembranen zijn veelbelovend voor de terugwinning van alkalisch afvalwater
Pervaporatiemembranen zijn veelbelovend voor de terugwinning van alkalisch afvalwater  Hoe gedragen deeltjes zich bij bevriezing?
Hoe gedragen deeltjes zich bij bevriezing?
 Koolstofputten in oude bossen overschat
Koolstofputten in oude bossen overschat Van de diepe mantel van de aarde, wetenschappers vinden een nieuwe manier waarop vulkanen ontstaan
Van de diepe mantel van de aarde, wetenschappers vinden een nieuwe manier waarop vulkanen ontstaan Opnieuw heet:2020 vestigt opnieuw een wereldwijd temperatuurrecord
Opnieuw heet:2020 vestigt opnieuw een wereldwijd temperatuurrecord Maïs beter te gebruiken als voedsel dan biobrandstof, studie vondsten
Maïs beter te gebruiken als voedsel dan biobrandstof, studie vondsten Hoe lang blijft een vlinder in een pop?
Hoe lang blijft een vlinder in een pop?
Hoofdlijnen
- Wanneer een zaadje in een plant spruit?
- Waarvoor stelde Lamarck een wetenschappelijke verklaring voor en waarom?
- Wat wordt bedoeld met 99 procent bepaling van ethylacetaat?
- Beschrijf en geef een voorbeeld van twee symbiotische relaties die zich voordoen tussen populaties in een gemeenschap?
- Welke epidermale lagen bevatten Langerhans -cellen?
- Wie heeft zelfstandige naamwoorden uitgevonden?
- Wat betekent verkiezing in de wetenschap?
- Waarom Twitter president Donald Trump niet zal verbieden
- Onderzoekers gebruiken modelleringstools voor machinaal leren om de technologie voor het bewerken van zinkvingernucleases te verbeteren
- Glycanen gevonden binding aan zoogdier-RNA

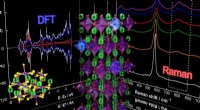
- Decodering van de structuur en eigenschappen van nabij-infrarood reflecterende pigmenten
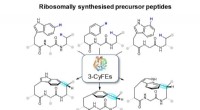
- Onderzoekers identificeren post-translationele vorming van gespannen cyclofanen in bacteriën
- Eigenschappen van spinnenzijde geanalyseerd voor gebruik als biogebaseerde vezels in de medische sector

- Chemici zien een vluchtige overgangstoestand van een reactie

 Controle over de Amerikaanse senaat:wat leert de geschiedenis ons over de mate waarin het de wetgevende beleidsvorming beïnvloedt?
Controle over de Amerikaanse senaat:wat leert de geschiedenis ons over de mate waarin het de wetgevende beleidsvorming beïnvloedt? Het begrijpen van secundaire lichtemissie door plasmonische nanostructuren kan medische beeldvorming verbeteren
Het begrijpen van secundaire lichtemissie door plasmonische nanostructuren kan medische beeldvorming verbeteren Hoe de aarde voor ET verbergen? Enorme lasers
Hoe de aarde voor ET verbergen? Enorme lasers  Latere tropische bloemen kunnen het zeeleven aantasten
Latere tropische bloemen kunnen het zeeleven aantasten Welke factoren moeten gelijk zijn bij een omkeerbare chemische reactie bij evenwicht?
Welke factoren moeten gelijk zijn bij een omkeerbare chemische reactie bij evenwicht?  Welke elektronen zijn de volant van het atoom?
Welke elektronen zijn de volant van het atoom?  Een zygoot bestaat uit elk 23 chromonen bij reproductie?
Een zygoot bestaat uit elk 23 chromonen bij reproductie?  Welke grens wordt gevormd wanneer Magma naar de oppervlakte stijgt en nieuwe korst wordt gevormd?
Welke grens wordt gevormd wanneer Magma naar de oppervlakte stijgt en nieuwe korst wordt gevormd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

