
Wetenschap
Wat is de molariteit van 10,0 g KCl in een oplossing van 0,500 L?
Hier leest u hoe u de molariteit van een KCL -oplossing kunt berekenen:
1. Bereken de mol KCl
* Molaire massa van KCl: 39.10 g/mol (k) + 35,45 g/mol (CL) =74,55 g/mol
* mol KCl: (10,0 g KCl) / (74,55 g / mol) =0,134 mol KCl
2. Bereken de molariteit
* molariteit (m) =mol opgeloste stof / liters van oplossing
* molarity = (0,134 mol kcl) / (0.500 l) = 0,268 m
Daarom is de molariteit van de KCL -oplossing 0,268 m.
Hoofdlijnen
- Wat gebeurt er als eerste messager-RNA of transfer-RNA?
- Oude fossielen van reuzenschildpadden gevonden in de Colombiaanse Andes
- Hoe wordt het genoemd als wetenschappers hun experiment meer dan eens worden getest?
- Waterkrachtdammen zorgen voor wijdverbreide uitsterving van soorten op de Amazone-woudeilanden
- Wat betekent biologische barrières?
- Wat is een primaire amine?
- Australische hagedissen eisen tol van schildpadeieren
- Wie zijn wetenschappers die vaccins ontwikkelen?
- Lymphatic System Science Activities
- Het ontcijferen van krachtige DNA-toxinegeheimen
- Onderzoekers geven gasdetectie bij kamertemperatuur groen licht

- Afstotend onderzoek:marine ontwikkelt scheepscoatings om brandstof te verminderen, energiekosten

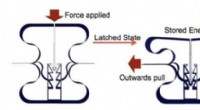
- Wetenschappers ontwerpen materiaal dat energie kan opslaan als een adelaarsgreep
- Neutronen inspecteren zouthoudende materialen om de opslag van afval op de lange termijn te verbeteren

 Wat is de FPS -eenheid van stroom?
Wat is de FPS -eenheid van stroom?  Wat is de betekenis van PDX -draad?
Wat is de betekenis van PDX -draad?  Koppeltekens in papieren titels zijn schadelijk voor het aantal citaten en de impactfactoren van tijdschriften
Koppeltekens in papieren titels zijn schadelijk voor het aantal citaten en de impactfactoren van tijdschriften Europa's richtlijn voor hernieuwbare energie klaar om wereldwijde bossen te schaden
Europa's richtlijn voor hernieuwbare energie klaar om wereldwijde bossen te schaden Student Loan processor vertelt 16, 500 leners van datalek
Student Loan processor vertelt 16, 500 leners van datalek Hoe helpt culturele antropologie de wereld?
Hoe helpt culturele antropologie de wereld?  Hoe slangen een blauwdruk verloren voor het maken van ledematen
Hoe slangen een blauwdruk verloren voor het maken van ledematen  Wat is het verschil tussen een permanente magneet en een tijdelijke magneet?
Wat is het verschil tussen een permanente magneet en een tijdelijke magneet?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


