
Wetenschap
Hoeveel totale ionen zijn aanwezig in 347 g CACL2?
Hier leest u hoe u het totale aantal ionen in 347 g CaCl₂ kunt berekenen:
1. Bereken de mol CaCl₂:
* Molaire massa van CaCl₂: 40.08 g/mol (Ca) + 2 * 35,45 g/mol (CL) =110,98 g/mol
* mol CaCl₂: (347 g) / (110,98 g / mol) =3,13 mol
2. Bereken de mol ionen:
* Elk CACL₂ -molecuul dissocieert in 3 ionen: 1 ca²⁺ ion en 2 Cl⁻ -ionen.
* Totaal aantal ionen: 3.13 Mol Cacl₂ * 3 ionen/mol =9,39 mol ionen
3. Bereken het aantal ionen:
* Avogadro's nummer: 6.022 x 10²³ ionen/mol
* Totaal aantal ionen: 9.39 mol ionen * 6.022 x 10²³ IONS/mol = 5,66 x 10²⁴ IONS
Daarom zijn er ongeveer 5,66 x 10²⁴ ionen aanwezig in 347 g CaCl₂.
 Onderzoek biedt nieuwe inzichten in de behandeling van afgas van staalproductie
Onderzoek biedt nieuwe inzichten in de behandeling van afgas van staalproductie De wetenschap van statische schokken schokte de 21e eeuw binnen
De wetenschap van statische schokken schokte de 21e eeuw binnen  Millimoles converteren naar PPM
Millimoles converteren naar PPM  Wat is de oplosbaarheid van natriumnitraat in water?
Wat is de oplosbaarheid van natriumnitraat in water?  Onderzoekers rapporteren over live intracellulaire beeldvorming met nieuwe, voorwaardelijk actieve immunofluorescentieprobe
Onderzoekers rapporteren over live intracellulaire beeldvorming met nieuwe, voorwaardelijk actieve immunofluorescentieprobe
 Warme perioden in de 20e eeuw zijn niet ongekend tijdens de laatste 2, 000 jaar
Warme perioden in de 20e eeuw zijn niet ongekend tijdens de laatste 2, 000 jaar Talloze branden verspreidden zich van noord naar zuid in Oregon
Talloze branden verspreidden zich van noord naar zuid in Oregon Mysterie opgelost:hoe blijven tips van planten virusvrij?
Mysterie opgelost:hoe blijven tips van planten virusvrij?  Recordjaar voor Franse champagne bemoedigt druiventelers niet
Recordjaar voor Franse champagne bemoedigt druiventelers niet Migratie en vervelling beïnvloeden de manier waarop vogels van kleur veranderen
Migratie en vervelling beïnvloeden de manier waarop vogels van kleur veranderen
Hoofdlijnen
- Pelagische zeevogels vliegen in het oog van de storm wanneer ze worden geconfronteerd met extreme weersomstandigheden
- Hebben vogelgezang en menselijke spraak biologische wortels?
- Zou je eiwitten in cellen of eiwitten vinden?
- Hoe een evolutionaire boom te laten groeien
- Waarom wordt DNA getranscribeerd?
- Is het geslacht van een cel van belang in onderzoek?
- De vorming van de mannelijke geslachtscellen of sperma wordt een wat genoemd?
- Onderzoek naar superstil gemaakte DNA hints naar nieuwe manieren om cellen te herprogrammeren
- Wat is er tussen de pubis en ischium?
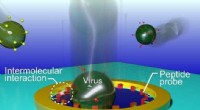
- Nieuwe virale identificatiemethode ontwikkeld
- Een efficiëntere, veiliger alternatief voor het inkopen van koper via bacteriën

- Robuuste en goedkope katalysatoren voor waterstofproductie

- Edelmetaalclusters kunnen de prestaties van katalysatoren verbeteren en hulpbronnen besparen

- Het onzichtbare spotten
 SpaceX lanceert geheime Zuma-missie
SpaceX lanceert geheime Zuma-missie Waarom een bewerkknop voor Twitter niet zo eenvoudig is als het lijkt
Waarom een bewerkknop voor Twitter niet zo eenvoudig is als het lijkt NASA stuurt voor het eerst Afro-Amerikaan naar ruimtestation
NASA stuurt voor het eerst Afro-Amerikaan naar ruimtestation Grafeen:200 keer sterker dan staal,
Grafeen:200 keer sterker dan staal,  Materialen voor supergeleidende qubits
Materialen voor supergeleidende qubits Streefdoelen klimaatakkoord Parijs uitgedaagd
Streefdoelen klimaatakkoord Parijs uitgedaagd Hoe weekdieren hun schelpen bouwen in de ijskoude wateren van Antarctica
Hoe weekdieren hun schelpen bouwen in de ijskoude wateren van Antarctica  Hallo, Alexa:Sorry dat ik je voor de gek hield
Hallo, Alexa:Sorry dat ik je voor de gek hield
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

