
Wetenschap
Wat is een voorbeeld van vloeistof voor het evenwicht van gasfaseverandering?
Hier is hoe het werkt:
* Verdamping: Watermoleculen aan het vloeibare oppervlak hebben voldoende energie om los te breken en de gasfase (waterdamp) in te gaan.
* condensatie: Tegelijkertijd botsen waterdampmoleculen in de lucht boven het vloeistof met het oppervlak en condenseren terug in de vloeibare fase.
evenwicht: De verdampingssnelheden en condens worden gelijk, wat betekent dat het aantal watermoleculen dat de gasfase binnenkomt gelijk is aan het aantal dat terugkeert naar de vloeibare fase. Dit creëert een dynamisch evenwicht waarbij de hoeveelheid vloeibaar water en waterdamp in de container constant blijft.
factoren die het evenwicht beïnvloeden:
* Temperatuur: Verhogende temperatuur is de verdamping voorstanders en verschuiven het evenwicht naar de gasfase.
* Druk: Het verhogen van de druk bevordert de condensatie, waardoor het evenwicht naar de vloeibare fase wordt verplaatst.
Visualisatie van het evenwicht:
Stel je een glas water voor met een deksel erop. Je kunt de waterdamp niet in de lucht boven het water zien, maar het is er. De snelheid van watermoleculen die aan de vloeistof ontsnappen, wordt in evenwicht gebracht door de snelheid van watermoleculen die terugkeren naar de vloeistof. Dit is een stabiele toestand en de hoeveelheden vloeistof en gas blijven relatief constant.
Dit voorbeeld toont de dynamische aard van het evenwicht, waar tegengestelde processen optreden met gelijke snelheden, wat resulteert in een schijnbaar onveranderlijke toestand.
 Wie experimenteerde met vloeistoffen en hoe ze reageren onder druk?
Wie experimenteerde met vloeistoffen en hoe ze reageren onder druk?  Wat zijn enkele eigenschappen van covalente kristallen?
Wat zijn enkele eigenschappen van covalente kristallen?  Nieuw, gladde toiletcoating zorgt voor schoner doorspoelen, bespaart water
Nieuw, gladde toiletcoating zorgt voor schoner doorspoelen, bespaart water Een atoom van een element heeft 54 protonen, sommige atomen van de elementen hebben 77 neutronen, terwijl andere 79 wat zijn atoomnummers en massa twee typen deze el?
Een atoom van een element heeft 54 protonen, sommige atomen van de elementen hebben 77 neutronen, terwijl andere 79 wat zijn atoomnummers en massa twee typen deze el?  Waarom is witte fosfor oplosbaar in cs2?
Waarom is witte fosfor oplosbaar in cs2?
 Geothermische energie:Boren van een 3, 000 meter diepe put
Geothermische energie:Boren van een 3, 000 meter diepe put Naschokken van de aardbeving van 1959 deed Yellowstone schudden in 2017-18
Naschokken van de aardbeving van 1959 deed Yellowstone schudden in 2017-18 Wat is de bron van warmte en licht voor alle planten?
Wat is de bron van warmte en licht voor alle planten?  Duitse rechtbank hoort beroep Peruaanse boeren tegen klimaatverandering
Duitse rechtbank hoort beroep Peruaanse boeren tegen klimaatverandering GPM vindt dat de regenval afneemt in extra-tropische storm Gabrielle
GPM vindt dat de regenval afneemt in extra-tropische storm Gabrielle
Hoofdlijnen
- Ouders van het jaar:Opruimende roofvogels tonen een hoog niveau van samenwerking bij het grootbrengen van kuikens
- Welke cel wordt waargenomen als A de vorming van een contractiele ring vertoont net voorafgaand aan cytoplasmatische divisie?
- Wat is kernen dat onstabiel verval heeft bekend als?
- Hoe definieerde Thomas Kuhn de normale wetenschap?
- Bestorming van het kasteel:nieuwe ontdekking in de strijd tegen bacteriën
- Vissenseks zo luid dat dolfijnen doof kunnen worden
- Waarom jouw voorouders het verspringen zouden hebben gedaan
- Wetenschappers roepen op tot actie om invasieve boomsoort aan te pakken
- Cassave beschermen tegen ziekten? Daar is een app voor
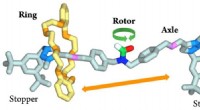
- Mechanica van het oneindig kleine:NanoGear, naar een moleculaire versnelling
- Onderzoekers pleiten voor hernieuwde focus op thermo-elektrische koeling

- Het degradatiegedrag van geavanceerde medische apparaten voorspellen

- Fotokatalysator maakt waterstofproductie 10 keer efficiënter
- Afval van het maken van paarse maïschips levert een natuurlijke kleurstof op, supplementen, kattenbakvulling

 Wat activeert een superzwaar zwart gat?
Wat activeert een superzwaar zwart gat?  Wat eten wilde vogels?
Wat eten wilde vogels?  Zal het einde van de COVID-19-pandemie een tweede Roaring 20s inluiden?
Zal het einde van de COVID-19-pandemie een tweede Roaring 20s inluiden? Het inzetten van onderzoek om maatschappelijke problemen op te lossen begint met het leggen van verbindingen en het maken van ruimte voor jongeren
Het inzetten van onderzoek om maatschappelijke problemen op te lossen begint met het leggen van verbindingen en het maken van ruimte voor jongeren  Milieugroenheid kan de testscores van studenten niet verbeteren, studie vondsten
Milieugroenheid kan de testscores van studenten niet verbeteren, studie vondsten Videogames strijden om de cloud terwijl de industrie zich inzet voor verandering
Videogames strijden om de cloud terwijl de industrie zich inzet voor verandering Polymeerfilm beschermt tegen elektromagnetische straling, signaal interferentie
Polymeerfilm beschermt tegen elektromagnetische straling, signaal interferentie AI recreëert het periodiek systeem der elementen van de chemie
AI recreëert het periodiek systeem der elementen van de chemie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

