
Wetenschap
Wat zijn enkele eigenschappen van covalente kristallen?
1. Sterke banden: Covalente kristallen hebben sterke covalente bindingen tussen de atomen, wat resulteert in een stijve en goed gedefinieerde structuur. De covalente bindingen worden gevormd door het delen van elektronen tussen atomen.
2. Hoge smelt- en kookpunten: Covalente kristallen hebben relatief hoge smelt- en kookpunten vanwege de sterke interatomaire krachten. De sterke covalente bindingen vereisen een aanzienlijke hoeveelheid energie om te breken, wat resulteert in hogere smelt- en kookpunten.
3. Isolatoren: Covalente kristallen zijn over het algemeen slechte geleiders van elektriciteit en worden geclassificeerd als isolatoren. De elektronen in covalente kristallen zijn sterk gelokaliseerd binnen de covalente bindingen tussen atomen, en er zijn geen vrije elektronen beschikbaar om elektrische stroom te geleiden.
4. Hardheid: Covalente kristallen kunnen hard zijn en bestand tegen vervorming, omdat de sterke covalente bindingen voorkomen dat de atomen gemakkelijk langs elkaar bewegen. Voorbeelden zijn onder meer diamant (covalent vast netwerk) en grafiet (covalent vast plaatmateriaal).
5. Oplosbaarheid: Covalente kristallen zijn doorgaans onoplosbaar in water en andere polaire oplosmiddelen vanwege hun niet-polaire aard. De covalente bindingen tussen atomen zijn niet-polair, waardoor ze niet goed interageren met polaire oplosmiddelen.
6. Lage elektrische geleidbaarheid: Zoals eerder vermeld zijn covalente kristallen slechte elektriciteitsgeleiders vanwege het gebrek aan vrije elektronen. De stevig gebonden elektronen in covalente bindingen voorkomen de beweging van ladingen.
7. Lage thermische geleidbaarheid: Covalente kristallen hebben een lage thermische geleidbaarheid, wat betekent dat ze slechte warmtegeleiders zijn. De sterke covalente bindingen en de stijve structuur belemmeren de overdracht van warmte door trillingen.
8. Reactiviteit: Covalente kristallen hebben over het algemeen een lagere reactiviteit vergeleken met ionische kristallen. Ze ondergaan niet gemakkelijk chemische reacties omdat de sterke covalente bindingen tussen atomen stabiel zijn en een hoge activeringsenergie vereisen om te verbreken.
9. Glanzend uiterlijk: Veel covalente kristallen vertonen een glanzend of glanzend uiterlijk vanwege de regelmatige rangschikking van atomen en de reflectie van licht op hun gladde oppervlakken.
10. Decolleté: Covalente kristallen vertonen vaak splitsingsvlakken, waarbij het kristal langs specifieke zwaktevlakken kan worden gesplitst. Deze zwaktevlakken treden op wanneer de covalente bindingen in bepaalde richtingen zwakker zijn.
 Wat is de chemische vergelijking wanneer ijzeroxide reageert met waterstofchloride?
Wat is de chemische vergelijking wanneer ijzeroxide reageert met waterstofchloride?  Kunstmatige cellen-in-cellen die door licht worden geactiveerd, fungeren als mini-chemische reactoren
Kunstmatige cellen-in-cellen die door licht worden geactiveerd, fungeren als mini-chemische reactoren Smartphonelab levert testresultaten in een oogwenk
Smartphonelab levert testresultaten in een oogwenk 99% van de microplastics in de oceaan 'verloren' om met kleurstof te worden geïdentificeerd?
99% van de microplastics in de oceaan 'verloren' om met kleurstof te worden geïdentificeerd?  Kleine sensoren ontwikkeld om de geheimen van hersenchemie te bestuderen
Kleine sensoren ontwikkeld om de geheimen van hersenchemie te bestuderen
Hoofdlijnen
- Wetenschappers ontdekken hoe parelmoer zichzelf assembleert tot een perfecte structuur
- Hoe bestrijden planten ziekten?
- Waarom is DNA de blauwdruk van het leven?
- Hoe katoen werd geboren
- Hoe reguleren PA-, ABA- en CBF-routes synergetisch de koudetolerantie van meloenen?
- No-till management kan de uitstoot van lachgas verminderen, klimaatverandering bestrijden
- Studenten zeggen dat ze een milieuvriendelijke manier hebben gevonden om Japanse kevers te vangen en te doden
- Hoe visvinnen evolueerden vlak voor de overgang naar land
- Wetenschappelijke naam voor een geslachtscel?
- Waterstof brandstofcellen:Met een database van 500, 000 materialen, onderzoekers kijken naar de beste weddenschappen

- Een niet-giftige lijm voor triplex—van glucose, citroenzuur

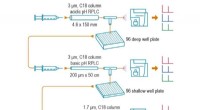
- Verbeterde eiwitanalyse kan vroege ziektedetectie helpen
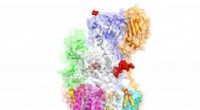
- Cryo-EM onthult kritisch eiwitmodificerend complex en potentieel medicijndoelwit
- Een manier bedenken om microplastics uit afvalwater te verwijderen - met okra, aloë

 Op afstand overleven:welke impact had werken op afstand op de psyche van werknemers?
Op afstand overleven:welke impact had werken op afstand op de psyche van werknemers?  Is NASCAR echt zo slecht voor het milieu?
Is NASCAR echt zo slecht voor het milieu?  Het begin van een nieuw tijdperk voor Supernova 1987a (update)
Het begin van een nieuw tijdperk voor Supernova 1987a (update) NASA-rover neemt monsters van actieve lineaire duin op Mars
NASA-rover neemt monsters van actieve lineaire duin op Mars Zullen aardbevingen ooit voorspelbaar zijn? | Hoe dingen werken
Zullen aardbevingen ooit voorspelbaar zijn? | Hoe dingen werken  Gepolariseerd licht - een eenvoudige route naar zeer chirale materialen
Gepolariseerd licht - een eenvoudige route naar zeer chirale materialen CRISPR-methode voor voorwaardelijke genregulatie
CRISPR-methode voor voorwaardelijke genregulatie Emissie-eigenaardigheden van hoog-kwantumopbrengst silicium nanodeeltjes
Emissie-eigenaardigheden van hoog-kwantumopbrengst silicium nanodeeltjes
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

