
Wetenschap
Wat gebeurt er als een chemische verandering niet door de voltooiing doorloopt?
1. Onvolledige reacties:
* Niet alle reactanten worden omgezet in producten: Sommige van de oorspronkelijke reactanten blijven niet -gereageerd.
* evenwicht: Deze toestand is dynamisch, wat betekent dat de voorwaartse en omgekeerde reacties met dezelfde snelheid plaatsvinden. Het is niet zo dat de reactie stopt; Het is dat de snelheden van de voorwaartse en omgekeerde reacties gelijk zijn.
2. Factoren die het evenwicht beïnvloeden:
* Temperatuur: Het veranderen van de temperatuur kan de voorwaartse of omgekeerde reactie bevorderen, waardoor het evenwichtspunt verschuift.
* concentratie: Het toevoegen van meer reactanten zal de reactie op productvorming duwen en vice versa.
* Druk: Voor reacties met gassen kan het veranderen van de druk de evenwichtspositie beïnvloeden.
3. Voorbeelden:
* Omkeerbare reacties: Veel chemische reacties zijn omkeerbaar, wat betekent dat ze in beide richtingen kunnen doorgaan. De reactie tussen waterstof en jodium om waterstofjodide te vormen bereikt bijvoorbeeld evenwicht wanneer wat waterstof en jodium niet -gereageerd blijven.
* Onvolledige verbranding: Het verbranden van brandstof in een beperkte zuurstoftoevoer kan leiden tot onvolledige verbranding, waardoor koolmonoxide en roets samen met koolstofdioxide worden geproduceerd.
4. Gevolgen:
* opbrengst: Onvolledige reacties leiden tot een lagere opbrengst van gewenste producten.
* onzuiverheden: Niet -gereageerde reactanten kunnen als onzuiverheden fungeren en de zuiverheid en eigenschappen van het eindproduct beïnvloeden.
* omkeerbaarheid: Evenwichtstoestanden maken de reactie omkeerbaar, wat betekent dat u mogelijk de omstandigheden moet aanpassen om de reactie verder naar voltooiing te sturen.
In wezen, wanneer een chemische verandering niet tot voltooiing gaat, betekent dit dat de reactie een dynamische balans heeft bereikt waarbij de snelheid van de voorwaartse reactie gelijk is aan de snelheid van de omgekeerde reactie. Deze evenwichtstoestand beïnvloedt de opbrengst, zuiverheid en omkeerbaarheid van de reactie.
Hoofdlijnen
- Wat is de officiële naam van de kleinste en eenvoudigste cellen?
- Welke van deze behoort niet Meissners Corpuseles Pacinian Corpuscles Merkerl -cellen Arieector Pili?
- Wat maakt iemand tweetalig? Er is geen eenvoudig antwoord
- Wat is mRNA? u moet op de hoogte zijn van het belangrijkste ingrediënt in sommige COVID-19-vaccins
- Trofische coherentie verklaart waarom netwerken weinig feedbacklussen en hoge stabiliteit hebben
- Welke F -waarde betekent in de microbiologie?
- Biologische leeftijd verklaart variatie in reacties op stress
- Percepties over wat er nodig is om te slagen in STEM-gebieden kunnen vrouwen buitensluiten
- Welk idee van Darwins op basis van fossielen en de moderne organismen die hij in feite heeft gevonden, zegt in feite dat genetische veranderingen door latere generaties worden geërfd?
- Transparante inkt gebruiken om kleurenafbeeldingen af te drukken

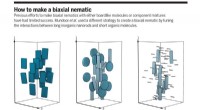
- Een nieuwe manier om biaxiale vloeibare kristallen in nematische fase te maken
- Massaproductie van geïndividualiseerde producten

- Een nieuwe gelelektroforesetechniek voor snelle biomarkerdiagnose via massaspectrometrie

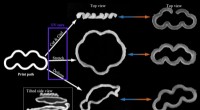
- Lab maakt 4D-printen praktischer
 De mogelijkheid om energie te gebruiken, voert vitale functies uit?
De mogelijkheid om energie te gebruiken, voert vitale functies uit?  Leg uit hoe materie kan worden ingedeeld in mengsels Pure stoffen verbindingen en elementen?
Leg uit hoe materie kan worden ingedeeld in mengsels Pure stoffen verbindingen en elementen?  Wiskunde onthult hoe vloeistofstroom bacteriën beïnvloedt
Wiskunde onthult hoe vloeistofstroom bacteriën beïnvloedt  Onderzoekers tonen de beste methoden om de met uitsterven bedreigde specht te helpen
Onderzoekers tonen de beste methoden om de met uitsterven bedreigde specht te helpen  Hebben kankercellen groeistimulerende signalen nodig?
Hebben kankercellen groeistimulerende signalen nodig?  De motivaties van mensen beïnvloeden de manier waarop ze informatie verzamelen
De motivaties van mensen beïnvloeden de manier waarop ze informatie verzamelen Wat houdt het fysieke proces van verdamping in?
Wat houdt het fysieke proces van verdamping in?  Uitbarsting van Kilauea stimuleert creatie van realtime luchtvervuilingsnetwerk
Uitbarsting van Kilauea stimuleert creatie van realtime luchtvervuilingsnetwerk
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


