
Wetenschap
Wat is diatomisch molecuul van een vaste verbinding?
* Diatomaire moleculen: Dit zijn moleculen gevormd uit twee atomen van hetzelfde element (zoals zuurstof, O2 of stikstof, N2).
* vaste verbindingen: Dit zijn stoffen waar meerdere elementen chemisch aan elkaar worden verbonden in een vaste verhouding, waardoor een rigide structuur wordt gevormd.
Het probleem: Vaste verbindingen vormen over het algemeen geen diatomaire moleculen. Ze vormen grotere, meer complexe structuren genaamd kristallen of roosters .
Voorbeeld: Natriumchloride (tafelzout, NaCl) is een vaste verbinding. Het is niet gemaakt van diatomaire NaCl -moleculen. In plaats daarvan heeft het een kristalstructuur waar natrium (Na+) en chloride (Cl-) ionen zijn gerangschikt in een herhaaldelijk patroon.
Mogelijke uitzonderingen:
* Sommige solide elementen kan bestaan als diatomaire moleculen in hun vaste structuur. Bijvoorbeeld, vaste witte fosfor (P4) is gemaakt van vier fosforatomen die aan elkaar zijn gebonden, maar die eenheden worden binnen de vaste stolte bij elkaar gehouden door zwakkere intermoleculaire krachten.
* Sommige vaste verbindingen kunnen diatomaire moleculen hebben als componenten. Moleculaire jodium (I2) bestaat bijvoorbeeld als diatomaire moleculen in zijn vaste vorm, maar de moleculen worden bij elkaar gehouden in een kristalrooster.
Conclusie: Hoewel het concept van een "diatomee molecuul van een vaste verbinding" geen standaardterm is, is het belangrijk om te begrijpen dat vaste verbindingen meestal niet bestaan als eenvoudige diatomaire moleculen. Ze vormen meer complexe structuren vanwege de aard van hun chemische binding.
 Waarom moet u uw omgeving aanpassen?
Waarom moet u uw omgeving aanpassen?  Aardobservaties helpen landen bij het beheren van hun waterveiligheid
Aardobservaties helpen landen bij het beheren van hun waterveiligheid Hoe te leven als een monnik in de westerse samenleving
Hoe te leven als een monnik in de westerse samenleving Wanneer virussen fytoplankton infecteren, het kan de wolken veranderen
Wanneer virussen fytoplankton infecteren, het kan de wolken veranderen Krill zou een geheim wapen kunnen zijn in de strijd tegen plastic in de oceaan
Krill zou een geheim wapen kunnen zijn in de strijd tegen plastic in de oceaan
Hoofdlijnen
- Nieuw onderzoek helpt de genetische basis te verklaren waarom we er zo uitzien
- Wat zijn enkele fysieke aanpassingen voor een kraai?
- Uit internationaal onderzoek blijkt hoe de 'bewaker' van het genoom werkt
- Wat is de dectiteit?
- Leg uit hoe DNA in de kern kan worden gerelateerd aan eiwitten en worden gemaakt ribosoom omvat hoe mutaties van invloed kunnen zijn op eiwitten?
- Onderzoek van moleculaire componenten die verantwoordelijk zijn voor het genereren van de actiepotentiaal in de Flytrap van Venus
- Wat is het enzym voor een eiwitsubstraat?
- Welk type weefselontwikkeling bestaat er in niet-vasculaire planten?
- Wordt Latijn nog steeds gebruikt in de wetenschap?
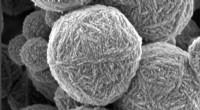
- Colloïdale gels, alomtegenwoordig in alledaagse producten, hun geheimen prijsgeven
- Polymeercoating koelt gebouwen af

- Mechanische huid maken

- Winnaars van een wedstrijd van $ 20 miljoen maken beton om koolstofdioxide op te vangen

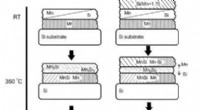
- Natuurkundigen houden toezicht op de vorming van hogere mangaansilicidefilms
 Switch-in-a-cell elektriseert het leven
Switch-in-a-cell elektriseert het leven Tanzaniaanse boeren stimuleren diëten, geestelijke gezondheid met duurzame methoden
Tanzaniaanse boeren stimuleren diëten, geestelijke gezondheid met duurzame methoden Poeders tonen hun kracht
Poeders tonen hun kracht  Schadelijke aardbevingen in Sichuan in verband met fracking-operaties
Schadelijke aardbevingen in Sichuan in verband met fracking-operaties Welke wet is Newton het meest bekend?
Welke wet is Newton het meest bekend?  Effecten van zichtbare lichtstraling
Effecten van zichtbare lichtstraling  Het is een mooie dag in de buurt... of toch niet?
Het is een mooie dag in de buurt... of toch niet? Wilt u de intellectuele ontwikkeling van uw kind stimuleren? Gebruik audioboeken in plaats van video's, zegt onderzoeker
Wilt u de intellectuele ontwikkeling van uw kind stimuleren? Gebruik audioboeken in plaats van video's, zegt onderzoeker
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

