
Wetenschap
Wat zijn de 6 kenmerken van gas?
1. onbepaalde vorm en volume: Gassen nemen de vorm en het volume van hun container aan. Dit komt omdat de deeltjes in een gas erg ver uit elkaar liggen en vrij bewegen.
2. Compressibiliteit: Gassen kunnen gemakkelijk worden gecomprimeerd, wat betekent dat hun volume kan worden verminderd door druk uit te oefenen. Dit is opnieuw te wijten aan de grote ruimtes tussen gasdeeltjes.
3. Lage dichtheid: Gassen hebben een lage dichtheid in vergelijking met vloeistoffen en vaste stoffen. Dit komt omdat de deeltjes zich over een veel groter volume verspreiden.
4. Uitbreiding: Gassen breiden zich uit om het gehele volume van hun container te vullen. Dit komt door de constante beweging en botsing van gasdeeltjes.
5. Vloeistofachtig gedrag: Gassen stromen gemakkelijk en kunnen worden gegoten. Dit houdt verband met het vrije verkeer van gasdeeltjes.
6. Diffusie: Gassen mengen gemakkelijk met elkaar door de constante willekeurige beweging van hun deeltjes. Dit is de reden waarom bijvoorbeeld de geur van kooktjes zich door een kamer verspreidt.
Het is belangrijk op te merken dat deze kenmerken vereenvoudigde verklaringen zijn. Het gedrag van echte gassen kan complexer zijn en beïnvloed worden door factoren zoals temperatuur, druk en het specifieke gas.
 Experts op het gebied van voedselsysteemplanning zeggen dat het tijd is om na te denken over de inspanningen van lokale overheden
Experts op het gebied van voedselsysteemplanning zeggen dat het tijd is om na te denken over de inspanningen van lokale overheden Bijenpollen maken voor bijen
Bijenpollen maken voor bijen NASA meet tropische storm Franklins doorweekte regen vanuit de ruimte
NASA meet tropische storm Franklins doorweekte regen vanuit de ruimte Technologische vooruitgang en het effect op het ecosysteem
Technologische vooruitgang en het effect op het ecosysteem Snelst groeiende planten voor een wetenschapsproject
Snelst groeiende planten voor een wetenschapsproject
Hoofdlijnen
- Wat is het directe resultaat van aerobe ademhaling?
- Hier ziet u hoe wetenschappers de genetische evolutie van COVID-19 volgen
- Wat worden de gegevens weergegeven in een cel?
- Platform op nanoschaal heeft tot doel de eiwitniveaus te beheersen
- Bij mensen welke van deze is vereist voor het dragen van zuurstof van de longen naar lichaamscellen?
- Wordt glycogenese een proces dat onmiddellijk na de maaltijd onmiddellijk voorkomt?
- Geef punten, advocaat Thst Biology is gekoppeld aan Physics Chemistry Mathsmatics Geography?
- Onderzoekers identificeren afweermechanisme van malariaparasiet
- In de genetische code worden sommige aminozuren niet gespecificeerd door codons?
- Nieuwe strategie om de verspreiding van zuurplaatsen in zeolieten te beheersen
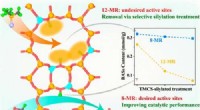
- De duikklokspin nabootsen om de omzetting van koolstof in brandstoffen te verbeteren

- Wetenschappers ontwikkelen mangaanoxidekatalysator met instelbare zuurgraad en selectiviteit

- Ionen in gesmolten zouten kunnen tegen de stroom in gaan

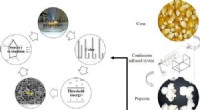
- Grote, smakelijke popcornpitten met infrarood koken
 Kīlauea lavabrandstoffen fytoplankton bloeien voor het eiland Hawaï
Kīlauea lavabrandstoffen fytoplankton bloeien voor het eiland Hawaï Een vulkaanexperiment maken voor kinderen
Een vulkaanexperiment maken voor kinderen Wat is de naam gegeven aan kleine klomp positief materiaal in het midden van een atoom?
Wat is de naam gegeven aan kleine klomp positief materiaal in het midden van een atoom?  Is Ceres de grootste van een asteroïde of een komeet?
Is Ceres de grootste van een asteroïde of een komeet?  Wie is eigenaar van archeologische artefacten?
Wie is eigenaar van archeologische artefacten?  Het ambitieuze voorstel om het noordpoolgebied opnieuw te bevriezen
Het ambitieuze voorstel om het noordpoolgebied opnieuw te bevriezen  Wat maakt zuur tot base en base?
Wat maakt zuur tot base en base?  Hoeveel ponden zijn er in 0,460 kilogram?
Hoeveel ponden zijn er in 0,460 kilogram?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

