
Wetenschap
Wat maakt zuur tot base en base?
Zuren:
1. Definitie: Een zuur is een stof die, wanneer opgelost in water, waterstofionen (H+) vrijgeeft en de concentratie van waterstofionen in de oplossing verhoogt.
2. Belangrijkste kenmerken:
- Zure smaak:Zuren hebben doorgaans een zure smaak. Citroensap en azijn zijn bijvoorbeeld zure stoffen.
- pH-waarde:Zuren hebben een pH-waarde lager dan 7 op de pH-schaal. Hoe lager de pH-waarde, hoe sterker de zuurgraad.
- Reactiviteit met metalen:Zuren reageren met bepaalde metalen, zoals ijzer of zink, om waterstofgas te produceren. Deze reactie staat bekend als een zuur-metaalreactie.
- Wordt blauw lakmoespapier rood:Zuren veranderen de kleur van blauw lakmoespapier in rood. Lakmoespapier is een indicator die van kleur verandert in de aanwezigheid van zuren of basen.
Basis:
1. Definitie: Een base is een stof die, wanneer opgelost in water, hydroxide-ionen (OH-) vrijgeeft en de concentratie van hydroxide-ionen in de oplossing verhoogt.
2. Belangrijkste kenmerken:
- Bittere smaak:Basen hebben vaak een bittere smaak. Zuiveringszout (natriumbicarbonaat) is bijvoorbeeld een basis en heeft een licht bittere smaak.
- pH-waarde:Basen hebben een pH-waarde groter dan 7 op de pH-schaal. Hoe hoger de pH-waarde, hoe sterker de basiciteit.
- Glad gevoel:de basis voelt glad aan bij aanraking. Dit komt door de vorming van zeepachtige stoffen wanneer basen reageren met oliën en vetten.
- Wordt rood lakmoespapier blauw:Basissen veranderen de kleur van rood lakmoespapier in blauw.
3. Neutralisatiereacties:
Zuren en basen ondergaan een chemische reactie die bekend staat als neutralisatie. Bij deze reactie reageren een zuur en een base in specifieke verhoudingen om zout en water te vormen. Het resulterende zout heeft een neutrale pH-waarde van ongeveer 7.
Samenvattend is een zuur een stof die waterstofionen (H+) in water afgeeft, een zure smaak heeft, een pH lager dan 7, en blauw lakmoespapier rood kleurt. Een base daarentegen geeft hydroxide-ionen (OH-) af in water, heeft een bittere smaak, een pH groter dan 7, en kleurt rood lakmoespapier blauw. Zuren en basen spelen een cruciale rol in verschillende chemische processen en worden veel gebruikt in het dagelijks leven, van huishoudelijke producten tot industriële toepassingen. Het begrijpen van hun eigenschappen en gedrag is van fundamenteel belang in veel wetenschappelijke disciplines.
Hoofdlijnen
- Hogere biodiversiteit door rivierverruimende maatregelen
- Onderzoekers brengen meerkat-chit-chat in kaart
- Wat bevatten eiwitten op elementair niveau?
- Hoe organismen de ruis filteren om nauwkeurige voorspellingen te doen
- Onderzoek levert inzicht op in hoe plantencellen groeien
- Interessante feiten over plantencellen
- Studie onderzoekt conflict tussen boeren en roofdieren
- Selenium zou de sleutel kunnen zijn tot het mysterie van kribbebijten bij paarden
- Hoe onze eencellige familieleden hun DNA verpakken
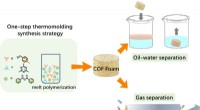
- Gebruik van smeltpolymerisatie om robuust covalent organisch raamwerkschuim te fabriceren
- Synthetische koolhydraten weren pneumokokkeninfecties af

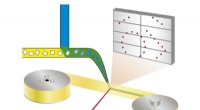
- Nieuwe methode maakt geautomatiseerd snel onderzoek van enzymatische processen mogelijk
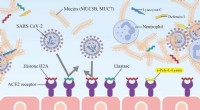
- Nieuwe sleutelbescherming tegen COVID-19 gevonden in speeksel
- Nieuwe methode kan scheuren in metaal opsporen lang voordat ze catastrofes veroorzaken

 Het langetermijneffect van bosbranden in Canada:Q en A
Het langetermijneffect van bosbranden in Canada:Q en A Het moleculaire schild:hoe theeplanten droogte bestrijden door eiwitfosforylering
Het moleculaire schild:hoe theeplanten droogte bestrijden door eiwitfosforylering  Nieuwe ultrahoge energiebron voor gammastraling gedetecteerd
Nieuwe ultrahoge energiebron voor gammastraling gedetecteerd 98% van de keizerspinguïnkolonies zou in 2100 uitgestorven kunnen zijn. Kan de bescherming van de Endangered Species Act hen helpen?
98% van de keizerspinguïnkolonies zou in 2100 uitgestorven kunnen zijn. Kan de bescherming van de Endangered Species Act hen helpen?  De groeiende markt voor 'oorlogsporno' - wat is er aan de hand?
De groeiende markt voor 'oorlogsporno' - wat is er aan de hand?  Experts:Slecht ontwerp, gebouw veroorzaakte gevaren bij de hoogste dam
Experts:Slecht ontwerp, gebouw veroorzaakte gevaren bij de hoogste dam Kweek koolstofvrije energie om klimaatdoelen te halen:analyse
Kweek koolstofvrije energie om klimaatdoelen te halen:analyse Wetenschapsprojecten op Centripetal Force
Wetenschapsprojecten op Centripetal Force
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


