
Wetenschap
Welk ISS is het totale reductiepotentieel van een cel waarin natrium (NA) wordt verminderd en zink (Zn) geoxideerd?
1. Identificeer de halfreacties
* reductie (bij de kathode): Na⁺ (aq) + e⁻ → na (s)
* oxidatie (bij de anode): Zn (s) → Zn²⁺ (aq) + 2e⁻
2. Zoek standaardreductiepotentialen op
U moet voor elke halfreactie de standaardreductiepotentialen (E °) vinden. Deze worden meestal aangetroffen in een tabel met standaardreductiepotentialen.
* na⁺ (aq) + e⁻ → na (s) E ° =-2,71 V
* Zn²⁺ (aq) + 2e⁻ → Zn (s) E ° =-0,76 V
3. Bepaal de totale celpotentiaal (E ° cel)
* Voor de celreactie wordt het reductiepotentiaal omgekeerd voor de oxidatiehalfreactie. Dit betekent dat we het negatieve van het standaardreductiepotentieel voor de zinkhalfreactie zullen gebruiken.
* Het totale celpotentiaal wordt berekend als:
E ° cel =E ° (reductie) + E ° (oxidatie)
E ° cel =-2,71 V + (+0,76 V)
E ° cel =-1,95 V
Conclusie
Het totale reductiepotentieel van de cel waarin natrium wordt verminderd en zink wordt geoxideerd, is -1,95 V . Deze negatieve waarde geeft aan dat de reactie niet spontaan is onder standaardomstandigheden.
 Onderzoekers kwantificeren voor het eerst wereldwijd verlies van fosfor door bodemerosie
Onderzoekers kwantificeren voor het eerst wereldwijd verlies van fosfor door bodemerosie Wat is het verschil tussen een das en een Wolverine?
Wat is het verschil tussen een das en een Wolverine?  Welke planeet heeft een storm die eeuwenlang heeft gewoed?
Welke planeet heeft een storm die eeuwenlang heeft gewoed?  Het herstellen van 30% van 's werelds ecosystemen in prioritaire gebieden kan uitsterven voorkomen en CO2 absorberen
Het herstellen van 30% van 's werelds ecosystemen in prioritaire gebieden kan uitsterven voorkomen en CO2 absorberen Twintig doden terwijl recordregens in Japan leiden tot massale evacuaties
Twintig doden terwijl recordregens in Japan leiden tot massale evacuaties
Hoofdlijnen
- Waarom hebben zich zoveel nieuwe ziekten ontwikkeld in de sector salades in zakken?
- Welk werk doet een cellichaam?
- Hoe de nederige zeekomkommer de viskweek zou kunnen transformeren
- Belangrijke foerageerplaatsen voor onechte karetschildpadden geïdentificeerd
- Wat is dactylologie?
- Een doorbraak voor snelle, efficiënte productie van menselijke immuuncellen
- Hoe polyfasische slaap werkt
- Thomas Hunt Morgan groepeerde de Drosophila -genen die werden ingehuurd in vier welke groepen?
- Technologie die complexe moleculaire interacties simuleert, kan leiden tot betere behandelingen voor kanker en COVID-19
- Vissen naar één slechte cel uit triljoenen goede

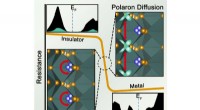
- Team werpt nieuw licht op ontwerp van anorganische materialen voor hersenachtige computers
- Wetenschappers ontwikkelen volledig door zonne-energie aangedreven autonome chemische minifabriek

- Ingenieurs bouwen chemisch aangedreven wielen die veranderen in tandwielen om mechanisch werk uit te voeren

- Reinigen zonder te schrobben en chemicaliën te gebruiken. Wetenschappers ontwikkelen zelfreinigend aluminium oppervlak

 Hersenziekten diagnosticeren? Een massaspectrometriebeeldvorming kan u op een dag helpen
Hersenziekten diagnosticeren? Een massaspectrometriebeeldvorming kan u op een dag helpen Hoeveel schade kan een mogelijke vulkaanuitbarsting in IJsland veroorzaken?
Hoeveel schade kan een mogelijke vulkaanuitbarsting in IJsland veroorzaken?  criminoloog, studententeam bouwt database op over schietpartijen op scholen in de VS
criminoloog, studententeam bouwt database op over schietpartijen op scholen in de VS Harvard nodigt eerstejaars uit op de campus, maar lessen blijven online
Harvard nodigt eerstejaars uit op de campus, maar lessen blijven online Raadsels in tijd en ruimte
Raadsels in tijd en ruimte Op origami geïnspireerde robot kan meeliften met een rover
Op origami geïnspireerde robot kan meeliften met een rover Opinie:De ware schade van invasieve uitheemse soorten is zojuist onthuld in een baanbrekend rapport – hier is hoe we moeten handelen
Opinie:De ware schade van invasieve uitheemse soorten is zojuist onthuld in een baanbrekend rapport – hier is hoe we moeten handelen  NASA-animatie volgt het einde van Tropical Storm Delta
NASA-animatie volgt het einde van Tropical Storm Delta
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

