
Wetenschap
Wat zijn de niet -polaire banden van SIH4?
SIH4 (Silane) heeft alleen niet -polaire bindingen .
Dit is waarom:
* Elektronegativiteitsverschil: Silicium (SI) en waterstof (H) hebben vergelijkbare elektronegativiteitswaarden (SI:1,90, H:2.20). Het verschil in elektronegativiteit is erg klein, wat betekent dat de elektronen in de Si-H-bindingen bijna gelijk worden gedeeld tussen de twee atomen.
* Symmetrie: De tetraëdrische geometrie van SIH4 zorgt ervoor dat de binddipolen (die erg klein zijn vanwege het elektronegativiteitsverschil) elkaar annuleren.
Daarom, hoewel elke Si-H-binding technisch enigszins polair is, is het totale molecuul niet-polair vanwege de symmetrie en minimale polariteit van de individuele bindingen.
 De watertoekomst van de derde pool van de aarde
De watertoekomst van de derde pool van de aarde Beter gebruik maken van aardobservaties om terrestrische en mariene ecosystemen te verbeteren
Beter gebruik maken van aardobservaties om terrestrische en mariene ecosystemen te verbeteren Zeegras bespaart stranden en geld
Zeegras bespaart stranden en geld Lenteregens zijn een verrassende bron van stuifmeel
Lenteregens zijn een verrassende bron van stuifmeel Eerste gedetailleerde simulatie van een aardbeving met megathrust in 2004
Eerste gedetailleerde simulatie van een aardbeving met megathrust in 2004
Hoofdlijnen
- De voedingsstof die het grootste percentage van het lichaam vormt, is?
- Vroege systemen voor classificerende planten waren gebaseerd op kenmerken die mensen gemakkelijk konden zien omdat?
- Hoe wordt gecompliceerd geërfd gedrag genoemd?
- Produceren zowel lichte reacties als de Calvin-cyclus driemoolstofsuikers?
- Een aanpassing om het oppervlak van een deelcel te vergroten die betrokken is bij cellulaire ademhaling?
- Indringende vraag:Wat is zaadbankieren?
- Studie brengt in kaart hoe genen de nieren instrueren om zich anders te ontwikkelen bij muizen en mensen
- Hoe vakantiefoto's van zebra's en walvissen het behoud kunnen helpen
- Welke klassen van biologische macromoleculen waartoe enzymen en zetmeel behoren?
- Studie biedt nieuwe inzichten voor technologieën voor het verzamelen van de zon

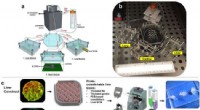
- Wetenschappers ontwikkelen body-on-a-chip-systeem om het testen van nieuwe medicijnen te versnellen
- Chemici ontwikkelen methode om snel te screenen, nauwkeurig fentanyl en een breed scala aan andere drugsmisbruiken identificeren

- Slim water kan helpen bij het terugwinnen van olie
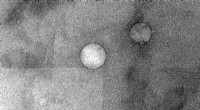
- Een moleculaire blik op ontluikende HDL-vorming

 Wat kunt u faciliteren?
Wat kunt u faciliteren?  Three Main Types of Galaxies
Three Main Types of Galaxies Wat is de afstand tussen 45 graden ten noorden en 30 minuten ten noorden?
Wat is de afstand tussen 45 graden ten noorden en 30 minuten ten noorden?  Ontdekking van een nieuwe oude reuzenslang in India
Ontdekking van een nieuwe oude reuzenslang in India  Gemengde bodembedekkers leggen koolstof vast in de bodem en kunnen de klimaatverandering helpen verminderen
Gemengde bodembedekkers leggen koolstof vast in de bodem en kunnen de klimaatverandering helpen verminderen Waarom hebben isotopen van niet -opgeladen elementen verschillende cijfers?
Waarom hebben isotopen van niet -opgeladen elementen verschillende cijfers?  Planten in Estuary Biomes
Planten in Estuary Biomes  Oplosbaar ijzer in de lucht boven Chinese steden kan gezondheidsrisico's opleveren, studie vondsten
Oplosbaar ijzer in de lucht boven Chinese steden kan gezondheidsrisico's opleveren, studie vondsten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

