
Wetenschap
Wat zijn drie soorten chemische reacties?
1. Synthesereacties: Deze reacties omvatten de combinatie van twee of meer reactanten om een enkel product te vormen. Ze worden vaak weergegeven als:
A + B → AB
* Voorbeeld: De vorming van water uit waterstof en zuurstof:
2h₂ + o₂ → 2h₂o
2. Ontledingsreacties: Dit zijn het tegenovergestelde van synthesereacties. Ze omvatten de afbraak van een enkele reactant in twee of meer producten.
AB → A + B
* Voorbeeld: De ontleding van calciumcarbonaat in calciumoxide en koolstofdioxide:
Caco₃ → Cao + Co₂
3. Verbrandingsreacties: Deze reacties omvatten de snelle reactie tussen een stof met een oxidatiemiddel, meestal zuurstof, om warmte en licht te produceren.
* Voorbeeld: Het verbranden van hout in aanwezigheid van zuurstof:
C₆h₁₂o₆ + 6o₂ → 6co₂ + 6h₂o + energie
Dit zijn slechts enkele voorbeelden. Er zijn veel andere soorten chemische reacties, zoals enkele verplaatsing, dubbele verplaatsing en zuurbasisreacties.
 Hoe wordt water in Apot op een fornuis overal heet?
Hoe wordt water in Apot op een fornuis overal heet?  Wetenschappers hebben de oorsprong van de bouwstenen van het leven ontdekt
Wetenschappers hebben de oorsprong van de bouwstenen van het leven ontdekt Computationele tools en nieuwe strategieën maken het ontdekken van medicijnen efficiënter
Computationele tools en nieuwe strategieën maken het ontdekken van medicijnen efficiënter Wat is het verschil tussen een RPH en Ph.D?
Wat is het verschil tussen een RPH en Ph.D?  Waarom bewaar je natriumchloride in gekleurde flessen?
Waarom bewaar je natriumchloride in gekleurde flessen?
 Vier soorten regen
Vier soorten regen Dramatische vegetatieveranderingen in het verleden duiden op een sombere toekomst
Dramatische vegetatieveranderingen in het verleden duiden op een sombere toekomst Voor een betere toekomst, gebruik deze tijd om thuis groene gewoontes aan te leren
Voor een betere toekomst, gebruik deze tijd om thuis groene gewoontes aan te leren Chinese mensenrechtenadvocaten richten hun pijlen op smog
Chinese mensenrechtenadvocaten richten hun pijlen op smog NASA ziet een zwakkere, langgerekte tropische depressie Kai-Tak
NASA ziet een zwakkere, langgerekte tropische depressie Kai-Tak
Hoofdlijnen
- Wijzigingen in de Amerikaanse importregels voor honden:wat ze zijn en waarom belangrijk voor hondenmensen
- Gewijzigde nucleotiden die worden gebruikt in COVID-19-vaccins werken zoals ontworpen
- Geen zoetekauw meer? De wetenschap schakelt het verlangen naar suiker bij muizen uit
- 10 fysieke menselijke eigenschappen die door de evolutie achterhaald zijn
- Uit onderzoek blijkt hoe RNA-‘junk’ onze genen controleert
- Ziekte van Lyme bij honden:wat hondeneigenaren moeten weten
- De neiging van de allelen op één chromosoom om samen te erven, wordt genoemd?
- Moeten alle chemosensorische modaliteiten worden verenigd in één zintuig?
- Wat is de relatie tussen eiwitten en DNA?
- De stress uit het in kaart brengen van restspanningen

- Technologische sprankje hoop voor de snowboardscene

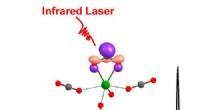
- Wetenschappers identificeren overgangsmetaal voor zeer efficiënte kooldioxide-activering
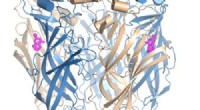
- Nieuwe moleculaire ontwerpen ontsluiten het therapeutisch potentieel van nicotinereceptoren
- Nieuwe geleiders met een hoog protonengehalte met inherent zuurstofarme lagen openen een duurzame toekomst
 School kan eng zijn tijdens een pandemie. Een nieuwe app helpt leraren weten hoe kinderen zich voelen
School kan eng zijn tijdens een pandemie. Een nieuwe app helpt leraren weten hoe kinderen zich voelen  Geef 10 voorbeelden van natuurlijke orderzin?
Geef 10 voorbeelden van natuurlijke orderzin?  De effecten van maansverduisteringen
De effecten van maansverduisteringen Uit onderzoek blijkt dat oesters door middel van filtratie kunnen helpen het rif schoon te maken
Uit onderzoek blijkt dat oesters door middel van filtratie kunnen helpen het rif schoon te maken  Wat zijn enkele interacties met de menselijke omgeving in Cuba?
Wat zijn enkele interacties met de menselijke omgeving in Cuba?  Hoogte of vlucht? Fossil beantwoordt enkele vragen over de evolutie van het vliegen bij dinosauriërs, maar roept andere op
Hoogte of vlucht? Fossil beantwoordt enkele vragen over de evolutie van het vliegen bij dinosauriërs, maar roept andere op  Is koolstofdioxide gemaakt van zuurstof?
Is koolstofdioxide gemaakt van zuurstof?  Afbeelding:De duisternis van de ruimte simuleren
Afbeelding:De duisternis van de ruimte simuleren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

