
Wetenschap
Welk atoom vertoont vergelijkbare eigenschappen als zuurstof?
Zuurstof en zwavel bevinden zich beide in Groep 16 (ook bekend als de chalcogenen) van het periodiek systeem. Elementen in dezelfde groep delen vergelijkbare chemische eigenschappen vanwege de aanwezigheid van hetzelfde aantal valentie-elektronen.
Zowel zuurstof als zwavel hebben zes valentie-elektronen en hebben de neiging twee elektronen te verkrijgen om een stabiele elektronenconfiguratie te bereiken. Dit maakt ze zeer reactief en vormt covalente bindingen met andere elementen om hun buitenste schil te voltooien.
Ze nemen gewoonlijk deel aan covalente binding om hun buitenste elektronenschillen te voltooien en niet-metaalachtige eigenschappen te demonstreren. Zuurstof en zwavel bestaan in verschillende allotrope vormen, waarbij zuurstof twee stabiele isotopen heeft en zwavel vier stabiele isotopen.
Bovendien vertonen zuurstof en zwavel een geleidelijke toename van hun atomaire en moleculaire afmetingen naarmate men lager in de groep komt, wat resulteert in een afname van de elektronegativiteit en ionisatie-energie.
 Ongeziene reizigers:stofstormen kunnen bacteriën en schimmels over de hele wereld verspreiden
Ongeziene reizigers:stofstormen kunnen bacteriën en schimmels over de hele wereld verspreiden  Hoe het onderzoek van rijke landen onze kennis van planten vertekent
Hoe het onderzoek van rijke landen onze kennis van planten vertekent  Welk dier doodt de meeste mensen? Hier is een onverwacht roofdier en hoe je jezelf kunt beschermen
Welk dier doodt de meeste mensen? Hier is een onverwacht roofdier en hoe je jezelf kunt beschermen  Onderzoekers identificeren vijf factoren voor betere strategieën voor kustrisicobeheer
Onderzoekers identificeren vijf factoren voor betere strategieën voor kustrisicobeheer Belangrijke ecosystemen van onderzeese canyons lopen gevaar
Belangrijke ecosystemen van onderzeese canyons lopen gevaar
Hoofdlijnen
- Wat is de basis voor het plaatsen van schimmels in verschillende phyla?
- Zijn er statistieken achter het succes van Pokémon Go?
- De menselijke cultuur verandert te snel om door de evolutie te kunnen worden bijgehouden. Hier ziet u hoe dit van invloed op u kan zijn
- Wat gebeurt er tijdens het transcriptieproces?
- Hoe de 'meesterregulatoren' van cellen DNA toegankelijk maken voor genexpressie
- Op de duikexpo in Thailand:angst voor de toekomst van koralen
- Nieuw onderzoek laat zien hoe sommige kippen gestreepte veren kregen
- Hoe beïnvloeden je hersenen je overlevingskansen in de wildernis?
- Waarom wordt klonen geclassificeerd als biotechnologie?
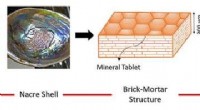
- Ontwikkeling van multifunctionele composietmaterialen voor ruimtevaarttoepassingen
- Nieuwe hout-metaalhybride voor lichtgewicht constructie

- Organische kristallen ijsvormende superkrachten

- Kunstmatige intelligentie versnelt fotodynamische simulaties

- Nieuwe studie stelt lage kosten voor, maskerontwerp met hoog rendement

 Wat zijn congruente vormen?
Wat zijn congruente vormen?  Dieren en planten in Griekenland
Dieren en planten in Griekenland Hoe technologie virusgeïnduceerde isolatie in Noorwegen aanpakt
Hoe technologie virusgeïnduceerde isolatie in Noorwegen aanpakt Overlevende orkanen, zeestijging in Keys kan leiden tot $ 3 miljard aan huisopkopen, verhogingen
Overlevende orkanen, zeestijging in Keys kan leiden tot $ 3 miljard aan huisopkopen, verhogingen Beroemde buitenissige golf nagebootst in laboratoriumspiegels Hokusais Great Wave
Beroemde buitenissige golf nagebootst in laboratoriumspiegels Hokusais Great Wave Het ontwikkelen van nieuwe methoden om antibiotica in groenten en regenwormen te detecteren
Het ontwikkelen van nieuwe methoden om antibiotica in groenten en regenwormen te detecteren  Nafta-gebruik
Nafta-gebruik  lasers, levitatie en machine learning maken betere hittebestendige materialen
lasers, levitatie en machine learning maken betere hittebestendige materialen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

