
Wetenschap
Hoeveel chloormoleculen zitten er in 134,5 gram chloor?
Om het aantal mol chloor in 134,5 gram te vinden, kunnen we de volgende formule gebruiken:
```
aantal mol =massa / molaire massa
```
Als we de gegeven waarden in de formule vervangen, krijgen we:
```
aantal mol =134,5 g / 70,9 g/mol =1,9 mol
```
Om tenslotte het aantal chloormoleculen in 1,9 mol chloor te vinden, kunnen we het getal van Avogadro gebruiken, dat ons vertelt dat er 6,022 x 10^23 moleculen in 1 mol van welke stof dan ook zitten. Als we het aantal mol vermenigvuldigen met het getal van Avogadro, krijgen we:
```
aantal moleculen =1,9 mol * 6,022 x 10^23 moleculen/mol =1,15 x 10^24 moleculen
```
Daarom zijn er 1,15 x 10^24 chloormoleculen in 134,5 gram chloor.
 Wat is de functie van het dehydrateren van calciumchloride bij het synthetiseren van tert-butylchloride?
Wat is de functie van het dehydrateren van calciumchloride bij het synthetiseren van tert-butylchloride?  Zonnepanelen met dunne schil bedrukt met inkjet
Zonnepanelen met dunne schil bedrukt met inkjet Identificatie van het enzym dat betrokken is bij stressmanagement in bacteriën
Identificatie van het enzym dat betrokken is bij stressmanagement in bacteriën Waarom is het moeilijker om een fusiereactie op gang te brengen dan een splijtingsreactie?
Waarom is het moeilijker om een fusiereactie op gang te brengen dan een splijtingsreactie?  Hoe kunnen zouten worden gevormd door astatine?
Hoe kunnen zouten worden gevormd door astatine?
Hoofdlijnen
- Waarom is UV-licht schadelijk?
- Wat is neutrofilis?
- Een botanisch mysterie opgelost door fylogenetische tests
- Evolutionair gewasonderzoek:Egoplanten geven lagere opbrengst
- Studie brengt in kaart hoe genen de nieren instrueren om zich anders te ontwikkelen bij muizen en mensen
- Nation-building of natuurvernietiging? Waarom het tijd is dat NZ de milieuschade van het koloniale verleden het hoofd moet bieden
- Alles wat je nooit wilde weten over bedwantsen, en meer
- Wat kunt u doen om uw gegevens op Facebook te beschermen?
- Vrijgen van genetische parasieten kan leiden tot nieuwe verdediging tegen gevaarlijke bacteriën
- Onderzoekers gebruiken zink om insulineproducerende cellen aan te vallen met regeneratief medicijn
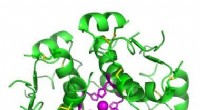
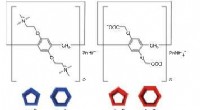
- Zelfsorterend door moleculaire geometrieën
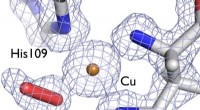
- Inzicht in 3D-structuur van enzymen kan biobrandstofkosten verlagen
- Uitvinding van 's werelds sterkste zilver

- Briljant ijzermolecuul zou kunnen zorgen voor goedkopere zonne-energie
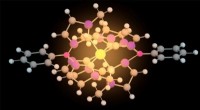
 Reinigen van Drusy Quartz
Reinigen van Drusy Quartz Wetenschappers demonstreren het potentieel van elektronenspin om kwantuminformatie over te dragen
Wetenschappers demonstreren het potentieel van elektronenspin om kwantuminformatie over te dragen  Natuurkundigen maakten een kristalrooster van polaritonen
Natuurkundigen maakten een kristalrooster van polaritonen Uit studentenevaluaties blijkt dat er sprake is van vooroordelen jegens vrouwelijke hoogleraren
Uit studentenevaluaties blijkt dat er sprake is van vooroordelen jegens vrouwelijke hoogleraren  Aardbevingsfout waarvan lang gedacht werd dat slapend Los Angeles zou kunnen verwoesten, onderzoekers zeggen:
Aardbevingsfout waarvan lang gedacht werd dat slapend Los Angeles zou kunnen verwoesten, onderzoekers zeggen: 20% korting berekenen
20% korting berekenen Nieuw model laat zien hoe buisvormige weefsels uniforme kanalen vormen
Nieuw model laat zien hoe buisvormige weefsels uniforme kanalen vormen  Google-app getest in Venezuela haalt uit naar perscensuur
Google-app getest in Venezuela haalt uit naar perscensuur
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

