
Wetenschap
Hoe vind je het aantal mol waterstof dat er in 3,5 NH42 CO3 zit?
Volg deze stappen om het aantal mol waterstof in 3,5 mol (NH4)2CO3 te vinden:
1. Bepaal de molaire verhouding van waterstof tot (NH4)2CO3. Uit de chemische formule (NH4)2CO3 zien we dat er 2 mol NH4+-ionen en 1 mol CO3^2--ionen per mol (NH4)2CO3 zijn. Elk NH4+-ion bevat 4 mol waterstofatomen.
2. Bereken het totaal aantal mol waterstof in 3,5 mol (NH4)2CO3. Vermenigvuldig het aantal mol (NH4)2CO3 met de molaire verhouding waterstof tot (NH4)2CO3.
$$ \text{Mollen van H} =3,5 \text{ mol (NH}_4)_2\text{CO}_3 \times \frac{8 \text{ mol H}}{1 \text{ mol (NH}_4 )_2\text{CO}_3 }$$ $$ \text{Mollen van H} =28 \text{ mol H}$$
Er zitten dus 28 mol waterstof in 3,5 mol (NH4)2CO3.
 Heeft Scott Pruitt goede argumenten voor het intrekken van de Clean Water Rule?
Heeft Scott Pruitt goede argumenten voor het intrekken van de Clean Water Rule?  Wat is het verschil tussen alkalinebatterijen en niet-alkalinebatterijen?
Wat is het verschil tussen alkalinebatterijen en niet-alkalinebatterijen?  Wetenschappers ontcijferen het belangrijkste principe achter de reactie van metallo-enzymen
Wetenschappers ontcijferen het belangrijkste principe achter de reactie van metallo-enzymen Spontane synthese van homogene polymeernetwerken
Spontane synthese van homogene polymeernetwerken De effecten van zout op ijsblokjes
De effecten van zout op ijsblokjes
 Ervaren dieren geluk?
Ervaren dieren geluk?  De langzame aardbevingen die we niet kunnen voelen, kunnen helpen beschermen tegen de verwoestende aardbevingen
De langzame aardbevingen die we niet kunnen voelen, kunnen helpen beschermen tegen de verwoestende aardbevingen Jair Bolsonaro kan worden gestopt met het vernietigen van de Amazone - hier hoe
Jair Bolsonaro kan worden gestopt met het vernietigen van de Amazone - hier hoe Monitoring van luchtvervuiling door branden
Monitoring van luchtvervuiling door branden Waarom heeft jouw boom dit najaar nog geen bladeren laten vallen, terwijl andere soortgelijke bomen dat wel hebben gedaan?
Waarom heeft jouw boom dit najaar nog geen bladeren laten vallen, terwijl andere soortgelijke bomen dat wel hebben gedaan?
Hoofdlijnen
- Wat is Nadph in fotosynthese?
- Waarom zijn sommige dieren moeilijker te klonen dan andere?
- Waarom zieke nertsen de zorgen over de vogelgriep doen herleven
- Waarom leven vrouwen langer dan mannen?
- Hoe rhizosfeermicro-organismen van een vlinderbloemige plant reageren op verandering
- Honden hoe oorlog werkt
- Dieren behandelen zichzelf met planten – een gedrag dat mensen al millennia lang observeren en nabootsen
- Is een perzikboom bloeiende of kegeldragende plant?
- Het verkennen van een oude gebeurtenis in pompoen, evolutie van kalebas en meloen
- Onderzoekers identificeren de innerlijke werking van cellulaire calciumpompen

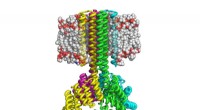
- Wetenschappers creëren vanuit het niets complexe transmembraaneiwitten
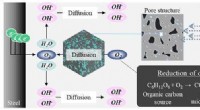
- Corrosiebestendigheid van stalen staven in beton bij vermenging met aerobe micro-organismen
- Wetenschappers hebben een alternatief gevonden voor waterchlorering

- Nieuwe verbindingen ontdekt in zeespons kunnen medicijnresistente bacteriën doden

 Wat beïnvloedt de atoomstraal?
Wat beïnvloedt de atoomstraal?  Vreemde zijde:waarom abseilende spinnen niet uit de hand lopen
Vreemde zijde:waarom abseilende spinnen niet uit de hand lopen  Waarom de alsem groeit:ecologen onderzoeken de overleving van dorre planten
Waarom de alsem groeit:ecologen onderzoeken de overleving van dorre planten  Kun je verslaafd zijn aan endorfine?
Kun je verslaafd zijn aan endorfine?  Overeenkomst van Parijs:vijf jaar later, het is tijd om de handel in koolstof op te lossen
Overeenkomst van Parijs:vijf jaar later, het is tijd om de handel in koolstof op te lossen Ingrediënten voor leven onthuld in meteorieten die op aarde vielen
Ingrediënten voor leven onthuld in meteorieten die op aarde vielen Besloten Facebook-groepen bieden rust voor gestresste vrouwen, maar het runnen ervan brengt nog meer onzichtbare arbeid met zich mee
Besloten Facebook-groepen bieden rust voor gestresste vrouwen, maar het runnen ervan brengt nog meer onzichtbare arbeid met zich mee Londen gaat oude auto's belasten om luchtvervuiling tegen te gaan
Londen gaat oude auto's belasten om luchtvervuiling tegen te gaan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

