
Wetenschap
Wat voor soort reactie vindt er plaats tussen calcium en EDTA?
Calciumionen en EDTA ondergaan een complexeringsreactie om een stabiel calcium-EDTA-complex te vormen. Deze reactie kan worden weergegeven als:
Ca²⁺ + EDTA⁴⁻ ⇌ CaEDTA²⁻
De evenwichtsconstante voor deze reactie is erg groot, wat aangeeft dat de reactie bijna voltooid is. Dit betekent dat bijna alle calciumionen in een oplossing een complex zullen vormen met EDTA als er voldoende EDTA aanwezig is.
De complexering van calcium door EDTA is belangrijk in veel biologische en industriële toepassingen. EDTA wordt bijvoorbeeld gebruikt als chelaatvormer om calciumionen uit water te verwijderen, en het wordt ook in de geneeskunde gebruikt om aandoeningen zoals hypercalciëmie (hoge calciumwaarden in het bloed) te behandelen.
 De limieten van Li-ion-batterijen uitbreiden - elektroden voor volledig solid-state batterijen
De limieten van Li-ion-batterijen uitbreiden - elektroden voor volledig solid-state batterijen Definitie van een mutatie in termen van moleculaire genetica
Definitie van een mutatie in termen van moleculaire genetica Wat is de chemische vergelijking voor baksteen?
Wat is de chemische vergelijking voor baksteen?  Stromend zout water over dit superhydrofobe oppervlak kan elektriciteit opwekken
Stromend zout water over dit superhydrofobe oppervlak kan elektriciteit opwekken Chemische reacties die betrokken zijn bij het bakken van een cake
Chemische reacties die betrokken zijn bij het bakken van een cake
 Nieuwe aanwijzingen helpen verklaren waarom PFAS-chemicaliën weerstand bieden aan sanering
Nieuwe aanwijzingen helpen verklaren waarom PFAS-chemicaliën weerstand bieden aan sanering Overwegverhuizingen:een case study waarom grote projecten ook investeringen in gezondheid moeten zijn
Overwegverhuizingen:een case study waarom grote projecten ook investeringen in gezondheid moeten zijn 'Geïmproviseerd, vlekkerig en laat':zal Californië zijn toezicht op de waterrechten hervormen?
'Geïmproviseerd, vlekkerig en laat':zal Californië zijn toezicht op de waterrechten hervormen?  Miljarden liters water bespaard door dunner wordende bossen
Miljarden liters water bespaard door dunner wordende bossen Klimaatverandering eist zijn tol van oceanen, ijs:VN-rapport
Klimaatverandering eist zijn tol van oceanen, ijs:VN-rapport
Hoofdlijnen
- Welke drie dingen zijn nodig om fotosynthese te laten plaatsvinden?
- Wat zijn biotische factoren in dit ecosysteem waarvan kikkers afhankelijk zijn?
- Uit Eurazië, een groot evolutionair knelpunt voor primaten?
- Wat is het verschil tussen een mens en een fruitvlieg?
- Worden we geboren met een moreel kompas?
- DNA-bewijs onthult twee vergeten Noord-Amerikaanse migraties
- Nieuwe AI-tool legt vast hoe eiwitten zich in context gedragen
- Is het leven begonnen in kleigrijze?
- Wiskundig model laat zien hoe zebravissen hun strepen krijgen
- De belangrijkste materialen en apparaten voor intrinsiek flexibele beeldschermen

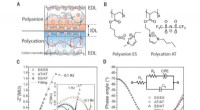
- Ionotronische technologie waarvoor geen vloeibare elektrolyten nodig zijn
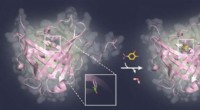
- Blokkeren van suikerstructuren op virussen en tumorcellen
- Deze hydrogeltablet kan een liter rivierwater in een uur zuiveren

- Exotische koolstofmicrokristallen in meteorietstof

 Wat zit er in de voedselketen van het regenwoud?
Wat zit er in de voedselketen van het regenwoud?  Voyager 2 bereikt interstellaire ruimte:wetenschappers detecteren sprong in plasmadichtheid
Voyager 2 bereikt interstellaire ruimte:wetenschappers detecteren sprong in plasmadichtheid Grammen omzetten in AMU
Grammen omzetten in AMU  De meest succesvolle startups combineren vriendschappen en zaken om teams te bouwen, onderzoek vindt
De meest succesvolle startups combineren vriendschappen en zaken om teams te bouwen, onderzoek vindt Rapport geeft 24 uur per dag inzicht in cyberaanvallen in Florida, ons
Rapport geeft 24 uur per dag inzicht in cyberaanvallen in Florida, ons Een evenwicht vinden in de antibioticageneeskunde:kunnen we slechte bacteriën doden en tegelijkertijd de goede behouden?
Een evenwicht vinden in de antibioticageneeskunde:kunnen we slechte bacteriën doden en tegelijkertijd de goede behouden?  Pulsar-timingarrays brengen ons dichter bij het ontdekken van superzware zwarte gaten
Pulsar-timingarrays brengen ons dichter bij het ontdekken van superzware zwarte gaten Hoe maak je een Streak-test met Rocks
Hoe maak je een Streak-test met Rocks
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

