
Wetenschap
Is zwaveldioxide een covalente verbinding?
In zwaveldioxide zijn het zwavelatoom en de twee zuurstofatomen covalent aan elkaar gebonden door elektronen te delen. Het zwavelatoom heeft zes valentie-elektronen en elk zuurstofatoom heeft zes valentie-elektronen. Om een stabiele elektronenconfiguratie te bereiken, deelt het zwavelatoom twee van zijn valentie-elektronen met elk van de zuurstofatomen, en deelt elk zuurstofatoom twee van zijn valentie-elektronen met het zwavelatoom. Dit resulteert in de vorming van twee covalente S-O-bindingen, elk bestaande uit een gedeeld elektronenpaar.
Als gevolg van dit delen van elektronen worden de zwavel- en zuurstofatomen in zwaveldioxide bij elkaar gehouden door sterke covalente krachten, wat aanleiding geeft tot de stabiliteit van het molecuul.
 Hoe heet de stof die een glowstick doet gloeien?
Hoe heet de stof die een glowstick doet gloeien?  Duurzaam, hoogwaardig papiercoatingmateriaal zou de vervuiling door microplastic kunnen verminderen
Duurzaam, hoogwaardig papiercoatingmateriaal zou de vervuiling door microplastic kunnen verminderen  Hoe verschillen de eigenschappen van aluminium- en koperatomen van hun ionen?
Hoe verschillen de eigenschappen van aluminium- en koperatomen van hun ionen?  Negatieve gezondheidseffecten van zure regen op mensen
Negatieve gezondheidseffecten van zure regen op mensen Waarom zou het toevoegen van HCL aan zuiver water het omzetten in een zuur?
Waarom zou het toevoegen van HCL aan zuiver water het omzetten in een zuur?
 Onderzoek laat zien hoe mosselen omgaan met vervuiling door microplastics
Onderzoek laat zien hoe mosselen omgaan met vervuiling door microplastics De klimaatcrisis als een terrorismekwestie bestempelen, zou tot actie kunnen leiden
De klimaatcrisis als een terrorismekwestie bestempelen, zou tot actie kunnen leiden Stoffen die worden gebruikt in huishoudelijke artikelen tasten het immuunsysteem van een kustmossel aan
Stoffen die worden gebruikt in huishoudelijke artikelen tasten het immuunsysteem van een kustmossel aan Risico op extreme weersomstandigheden groter als de doelstellingen van de Overeenkomst van Parijs niet worden gehaald
Risico op extreme weersomstandigheden groter als de doelstellingen van de Overeenkomst van Parijs niet worden gehaald Zijn de media allemaal kommer en kwel? Niet als het gaat om dekking van onze oceanen
Zijn de media allemaal kommer en kwel? Niet als het gaat om dekking van onze oceanen
Hoofdlijnen
- Wat is ureum?
- Soorten instrumenten die worden gebruikt voor het meten van lichaamstemperaturen
- Studie suggereert nieuwe doelen voor het verbeteren van het sojaoliegehalte
- Wetenschappers ontdekken hoe het belangrijkste enzym dat betrokken is bij veroudering, kanker assembleert
- Instrumenten die worden gebruikt in de biologie
- Wat is de betekenis van h20 in de wetenschap?
- Hoe dragen dieren zoals het afgebeelde hert bij aan de stikstofcyclus?
- Nieuwe celvrije eiwitkristallisatiemethode om structurele biologie te bevorderen
- Keizerspinguïns marcheren richting uitsterven?
- Onderzoek naar celisolatie levert veelbelovende resultaten op

- Metalen stimuleren een veelbelovende methode om schadelijke kooldioxide onder de zee te begraven

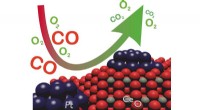
- Dynamische katalysatoren voor schone lucht in de stad
- Stampede2, Bridges-simulaties tonen zwakke plekken in Ebola-virus nucleocapsid

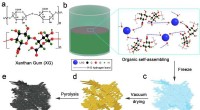
- Onderzoekers stellen nieuwe krachtige dual-ion-batterijen voor met een 3D-poreuze structuur
 Wetenschappers hebben gemeenschappelijke genen ontdekt die koffieplanten beschermen tegen verwoestende ziekten
Wetenschappers hebben gemeenschappelijke genen ontdekt die koffieplanten beschermen tegen verwoestende ziekten  Wetenschappers stellen een mogelijke methode voor voor beeldgestuurde synergetische kankertherapie
Wetenschappers stellen een mogelijke methode voor voor beeldgestuurde synergetische kankertherapie Globale temperatuurverandering toe te schrijven aan externe factoren, bevestigt nieuwe studie
Globale temperatuurverandering toe te schrijven aan externe factoren, bevestigt nieuwe studie Amerikanen worden echt gek van apparaten die ze volgen en afluisteren
Amerikanen worden echt gek van apparaten die ze volgen en afluisteren Wetenschappers ontdekken een exotisch kwantuminterferentie-effect in een topologisch isolatorapparaat
Wetenschappers ontdekken een exotisch kwantuminterferentie-effect in een topologisch isolatorapparaat  Typen instrumenten die worden gebruikt bij het meten van lichaamstemperatuur
Typen instrumenten die worden gebruikt bij het meten van lichaamstemperatuur Sporen van kruipen in Italiaanse grot geven aanwijzingen voor sociaal gedrag van oude mensen
Sporen van kruipen in Italiaanse grot geven aanwijzingen voor sociaal gedrag van oude mensen Eenvoudige manier om scheikundeformules te leren
Eenvoudige manier om scheikundeformules te leren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

