
Wetenschap
Welke massa is nodig om de 2N-oplossing van Na2co3 het natriumcarbonaat te laten berekenen dat zal worden opgelost in 500 ccc?
Hier willen we een 2N-oplossing maken. Dus normaliteit (N) =2
Gegeven volume =500 ml =0,5 l
De formule om het aantal benodigde mol opgeloste stof te berekenen is:
Aantal mol =Normaliteit × Volume van de oplossing in liters
Bereken eerst het aantal benodigde mol Na2CO3.
Aantal mol =Normaliteit × Volume van de oplossing in liters
=2 N × 0,5 L
=1 mol
We moeten 1 mol Na2CO3 oplossen in 500 ml water om een 2N-oplossing te maken.
Bereken nu de benodigde massa Na2CO3.
Molaire massa Na2CO3 =106 g/mol (natrium:2 × 23 g/mol, koolstof:1 × 12 g/mol, zuurstof:3 × 16 g/mol)
Massa =Aantal mol × Molaire massa
Massa =1 mol × 106 g/mol
=106 gram
Daarom moet 106 gram Na2CO3 worden opgelost in 500 ml water om een 2N-oplossing te maken.
 Is calciumwaterstofcarbonaat een zuurbase of neutraal?
Is calciumwaterstofcarbonaat een zuurbase of neutraal?  Meer elektronische materialen geopend met nieuw metaal-organisch raamwerk
Meer elektronische materialen geopend met nieuw metaal-organisch raamwerk Hoe inerte verbindingen ionen kunnen stelen
Hoe inerte verbindingen ionen kunnen stelen Is de combinatie tussen natrium en chloor om chloride te produceren een chemische reactie?
Is de combinatie tussen natrium en chloor om chloride te produceren een chemische reactie?  Zeer efficiënte en stabiele nabij-infraroodfosfor voor nachtzicht en bio-imaging
Zeer efficiënte en stabiele nabij-infraroodfosfor voor nachtzicht en bio-imaging
 Schatting van de volledigheid van de carbonaatlaag via stratigrafische voorwaartse modellering
Schatting van de volledigheid van de carbonaatlaag via stratigrafische voorwaartse modellering Mensen, stroomkosten houden indoor farming laag
Mensen, stroomkosten houden indoor farming laag Green Deal:Goed voor een klimaatneutraal Europa, slecht voor de planeet
Green Deal:Goed voor een klimaatneutraal Europa, slecht voor de planeet Gedurfde onderwatermissie onthult hoe diepe stromingen op de oceaanbodem duizenden kilometers kunnen afleggen
Gedurfde onderwatermissie onthult hoe diepe stromingen op de oceaanbodem duizenden kilometers kunnen afleggen Chemische reacties die betrokken zijn bij de groei van planten
Chemische reacties die betrokken zijn bij de groei van planten
Hoofdlijnen
- Vogelgezang en menselijke stem opgebouwd uit dezelfde genetische blauwdruk
- Wetenschapsprojecten over Dominant en Recessieve Genen
- Hoe zijn sterk gevouwen membranen een voordeel voor de functies van cellulaire delen?
- Rapport:Er zijn geen goede of slechte oliegewassen, alleen goede en slechte praktijken
- Factoren die de primaire productiviteit beïnvloeden
- Ontdekking werpt licht op hoe gewervelde dieren zien
- Hoe medicijnresistente ziekteverwekkerstammen elkaar ontmoeten en evolueren op bloembollen
- Belangrijkste factoren die bijdragen aan een hoge lokale diversiteit aan bomen van Euphorbiaceae in Xishuangbanna
- Drie redenen waarom de celdeling belangrijk is
- Website voor het delen van gegevens kan de reactie op nieuwe illegale drugs versnellen

- Prominente academici pleiten voor meer wetenschap in forensische wetenschap

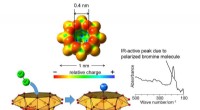
- Polarisatie van broommolecuul in vanadiumoxideclusterholte en nieuwe bromering van alkaan
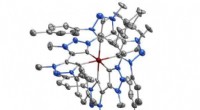
- Moderne alchemie creëert lichtgevende ijzermoleculen
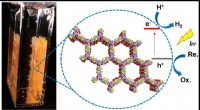
- Onderzoekers ontdekken zeer actieve organische fotokatalysator
 NASA selecteert nieuwe technologieën voor vliegtesten voor toekomstige ruimteverkenning
NASA selecteert nieuwe technologieën voor vliegtesten voor toekomstige ruimteverkenning Handsignalen verbeteren het succes van videovergaderingen
Handsignalen verbeteren het succes van videovergaderingen Nanomaterialen in zonnebrandmiddelen en boten maken het leven in de zee kwetsbaar
Nanomaterialen in zonnebrandmiddelen en boten maken het leven in de zee kwetsbaar Onderzoekers demonstreren op grafeen gebaseerde nano-elektromechanische periodieke array met afstembare frequentie
Onderzoekers demonstreren op grafeen gebaseerde nano-elektromechanische periodieke array met afstembare frequentie  Ondanks diepe staatsangsten toont onderzoek aan dat federale werknemers effectief en betrokken zijn, en niet subversief
Ondanks diepe staatsangsten toont onderzoek aan dat federale werknemers effectief en betrokken zijn, en niet subversief  Quantumcomputer:waren van plan er een te maken die werkt als een brein
Quantumcomputer:waren van plan er een te maken die werkt als een brein Een verbinding is wat of ionisch van aard?
Een verbinding is wat of ionisch van aard?  Orkaan Ian trekt aan tot categorie 4 terwijl hij richting Florida trekt
Orkaan Ian trekt aan tot categorie 4 terwijl hij richting Florida trekt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

