
Wetenschap
Welke informatie is nodig om de pH in een oplossing te berekenen?
1. Meten van de elektrische potentiaal van de oplossing met behulp van een pH-meter. Een pH-meter meet het spanningsverschil tussen een glaselektrode en een referentie-elektrode, dat evenredig is met de pH van de oplossing.
2. Gebruik pH-indicatorpapier of -strips. Deze worden behandeld met chemicaliën die van kleur veranderen bij verschillende pH-niveaus. Door de kleur van het papier of de strook te vergelijken met een kleurenkaart, kunt u de pH van de oplossing schatten.
3. Berekening van de pH uit de concentratie waterstofionen.
- Voor oplossingen van sterke zuren of basen kan de concentratie waterstofionen rechtstreeks worden berekend uit de concentratie van het zuur of de base met behulp van de dissociatieconstante (Ka of Kb).
- Voor oplossingen van zwakke zuren of basen kan de concentratie van waterstofionen worden berekend door de Henderson-Hasselbalch-vergelijking op te lossen. Deze vergelijking drukt de pH van een oplossing uit als functie van de concentratie van het zwakke zuur of de zwakke base en de dissociatieconstante ervan.
 Welke dranken barsten van het umami-potentieel?
Welke dranken barsten van het umami-potentieel? Een zuur heeft Ka 2,5 10 4 Wat is de Kb voor de geconjugeerde base hiervan bij 25 C Kw 1,0 14 C?
Een zuur heeft Ka 2,5 10 4 Wat is de Kb voor de geconjugeerde base hiervan bij 25 C Kw 1,0 14 C?  Hoe beïnvloedt de stikstofdynamiek de koolstof- en waterbudgetten in China?
Hoe beïnvloedt de stikstofdynamiek de koolstof- en waterbudgetten in China?  Hoe verandert de oplosbaarheid van zout met de temperatuur?
Hoe verandert de oplosbaarheid van zout met de temperatuur?  Onderzoekers maken gepantserde emulsies als kleine reageerbuisjes voor parallelle reacties
Onderzoekers maken gepantserde emulsies als kleine reageerbuisjes voor parallelle reacties
 Hoe u zanddollars op het strand kunt vinden
Hoe u zanddollars op het strand kunt vinden Video:plasticvervuiling in de oceaan vanuit de ruimte in de gaten houden
Video:plasticvervuiling in de oceaan vanuit de ruimte in de gaten houden Het verbranden van aardgas is nu gevaarlijker dan steenkool in Illinois, studie toont
Het verbranden van aardgas is nu gevaarlijker dan steenkool in Illinois, studie toont Hoe deelnemers aan wetenschappelijke conferenties hun ecologische voetafdruk kunnen verkleinen
Hoe deelnemers aan wetenschappelijke conferenties hun ecologische voetafdruk kunnen verkleinen  Figuren laten zien dat niet-inheemse soorten ecosystemen kunnen binnendringen door onverwachte partnerschappen te vormen
Figuren laten zien dat niet-inheemse soorten ecosystemen kunnen binnendringen door onverwachte partnerschappen te vormen
Hoofdlijnen
- Onderzoek naar rubberplantages op het eiland Hainan onthult geheimen van de bodem
- Hoe de ziekteverwekker Mycobacterium tuberculosis zijn enige bekende exotoxine uitscheidt en distribueert
- Welke soorten bindingen houden de basen bij elkaar om sport-DNA te creëren?
- Wat bevordert de opslag van glucose als glycogeen?
- Testen wijst uit dat Michigan-honden die ziek maken, parvovirus zijn
- Wat zijn de aanpassingen van bladepidermale cellen?
- Het dubbele leven van Sp1:een nieuwe rol van eiwitten zet het denken over de impact ervan op kanker op zijn kop
- Hoe eiwitten 'verborgen' DNA binden
- Maagdelijke vrouwelijke spinnen gevonden bereid om zichzelf over te geven om levend te worden opgegeten door spinnetjes
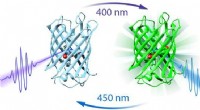
- Nieuwe techniek die laat zien hoe een eiwitlichtschakelaar werkt, kan biologisch onderzoek verbeteren
- Synthese van nieuwe rode fosforen met een slim materiaal als gastheermateriaal

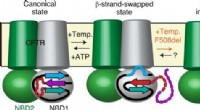
- Uiterlijk van cystische fibrose op moleculaire schaal
- Nieuw licht werpen op intensief bestudeerd materiaal

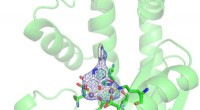
- Vooruitgang in de richting van een nieuwe griepbehandeling, dankzij een kleine aanpassing
 De perfecte zeef op atomaire schaal
De perfecte zeef op atomaire schaal Hoe Britse mensen uitzonderlijk koude winters doorstonden
Hoe Britse mensen uitzonderlijk koude winters doorstonden  Kan het leven op aarde overleven op Mars?
Kan het leven op aarde overleven op Mars?  Parasieten of niet? Transponeerbare elementen in fruitvliegjes
Parasieten of niet? Transponeerbare elementen in fruitvliegjes  Hoe wordt een blizzardstorm gevormd?
Hoe wordt een blizzardstorm gevormd?  Welzijnsvoorwaarde is niet effectief, auteurs van grote studie zeggen:
Welzijnsvoorwaarde is niet effectief, auteurs van grote studie zeggen: Hoe zou Einstein e-mail gebruiken? Brievenschrijvers van weleer hadden dezelfde correspondentiepatronen als e-mailgebruikers van nu
Hoe zou Einstein e-mail gebruiken? Brievenschrijvers van weleer hadden dezelfde correspondentiepatronen als e-mailgebruikers van nu  Zeldzaam schilderij van Picasso in Hong Kong voorafgaand aan historische veiling
Zeldzaam schilderij van Picasso in Hong Kong voorafgaand aan historische veiling
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

