
Wetenschap
De zuurgraad van een oplossing weerspiegelt de vrije waterstofionen in oplossing?
De zuurgraad of alkaliteit van een oplossing wordt bepaald door de concentratie waterstofionen (H+) die in de oplossing aanwezig zijn. Volgens de pH-schaal, die loopt van 0 tot 14, wordt een oplossing met een pH-waarde van 7 als neutraal beschouwd, wat duidt op een gelijke concentratie waterstofionen en hydroxide-ionen (OH-). Oplossingen met een pH-waarde lager dan 7 zijn zuur, wat een hogere concentratie waterstofionen betekent, terwijl oplossingen met een pH-waarde boven 7 basisch of alkalisch zijn, wat duidt op een lagere concentratie waterstofionen en een hogere concentratie hydroxide-ionen.
De vrije waterstofionen in oplossing zijn ervoor verantwoordelijk dat zure oplossingen hun karakteristieke eigenschappen krijgen, zoals zure smaak, het vermogen om te reageren met metalen en basen, en het vermogen om bepaalde indicatoren (zoals lakmoes) rood te maken. Hoe hoger de concentratie vrije waterstofionen, hoe sterker de zuurgraad van de oplossing.
 Hoe u het ionische percentage kunt berekenen zodra u het elektronegativiteitsverschil krijgt
Hoe u het ionische percentage kunt berekenen zodra u het elektronegativiteitsverschil krijgt Waarom wordt calciumoxide in de landbouw gebruikt om de zuurgraad van de bodem te verminderen?
Waarom wordt calciumoxide in de landbouw gebruikt om de zuurgraad van de bodem te verminderen?  Waarom complottheorieën kunnen fungeren als radicaliseringsvermenigvuldigers van extreemrechtse idealen
Waarom complottheorieën kunnen fungeren als radicaliseringsvermenigvuldigers van extreemrechtse idealen  Moleculaire trillingen benutten om geleidende polymeren te synthetiseren
Moleculaire trillingen benutten om geleidende polymeren te synthetiseren Hoe tropolonen in schimmels worden gesynthetiseerd:70 jaar oud chemisch mysterie opgelost
Hoe tropolonen in schimmels worden gesynthetiseerd:70 jaar oud chemisch mysterie opgelost
Hoofdlijnen
- Hoe het bewustzijn bij dieren onderzocht zou kunnen worden
- Hoe je hersenen werken
- Welk deel van een rode bloedcel geeft het de kleur en transporteert zuurstof?
- EU stemt ermee in om in 2018 meer vis op een duurzame manier te vangen
- Is gelelektroforese een belangrijk hulpmiddel dat in de biotechnologie wordt gebruikt voor forensisch onderzoek en vaderschapstests?
- Het simuleren van seks met walvisachtigen met kadaverdelen biedt inzicht in mariene copulatie
- Visa, MasterCard... DNA-kaart:wat zit er in je portemonnee?
- Migratie loont voor zangvogels
- Wetenschappers hebben het allereerste roestpathogeen gen geïsoleerd dat tarweplanten detecteren om resistentie in te schakelen
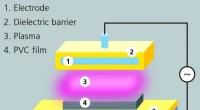
- Plasmabehandeling vermindert de migratie van weekmakers uit bloedzakken
- Onderzoek levert nieuw ontwerpprincipe op voor watersplitsende katalysatoren

- Steenademende bacteriën zijn elektron-spin-dokters, studie toont
- Flexibele kwantumzeef filtert de brandstof van ruimteschip Enterprise

- Biosensortechnologieën om effectievere benaderingen van ziektebehandeling te bieden

 Welk type water produceert schuim?
Welk type water produceert schuim?  Een nieuw apparaat voor het opsporen van gaslekken
Een nieuw apparaat voor het opsporen van gaslekken RNA-bewerkingstool een snelle, gevoelige test voor COVID-19
RNA-bewerkingstool een snelle, gevoelige test voor COVID-19 Beter kombucha brouwen door chemie
Beter kombucha brouwen door chemie  De ontdekking van Christmas Island hertekent de kaart van het leven
De ontdekking van Christmas Island hertekent de kaart van het leven Gifstoffen in oud speelgoed een obstakel voor circulaire economie
Gifstoffen in oud speelgoed een obstakel voor circulaire economie Astronomen volgen de geboorte van een superaarde
Astronomen volgen de geboorte van een superaarde Een litteken dat de Woolsey Fire achterliet
Een litteken dat de Woolsey Fire achterliet
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

