
Wetenschap
Welke soorten intermoleculaire krachten zijn aanwezig in een mengsel van calciumbromide en water?
1. Ion-dipoolkrachten :Deze krachten zijn aanwezig tussen de positief geladen calciumionen (Ca2+) en de polaire watermoleculen. De watermoleculen hebben een lichte negatieve lading vanwege de elektronegativiteit van zuurstof, en worden aangetrokken door de positieve lading van de calciumionen.
2. Dipool-dipoolkrachten :Deze krachten zijn aanwezig tussen de polaire watermoleculen. De watermoleculen hebben een permanent dipoolmoment vanwege het verschil in elektronegativiteit tussen zuurstof en waterstof. Het positieve uiteinde van het ene watermolecuul wordt aangetrokken door het negatieve uiteinde van een ander watermolecuul.
3. Waterstofbinding :Dit is een speciaal type dipool-dipoolkracht die optreedt wanneer een waterstofatoom covalent gebonden is aan een zeer elektronegatief atoom zoals zuurstof, stikstof of fluor. In het geval van calciumbromide en water vindt waterstofbinding plaats tussen de watermoleculen. Het waterstofatoom in het watermolecuul is covalent gebonden aan het zuurstofatoom en heeft een lichte positieve lading. Deze positieve lading wordt aangetrokken door de negatieve lading van het zuurstofatoom in een ander watermolecuul, waardoor een waterstofbrug ontstaat.
De combinatie van deze intermoleculaire krachten resulteert in de vorming van een stabiel mengsel van calciumbromide en water. De ionische krachten tussen de calciumionen en de watermoleculen zijn sterk, en de dipool-dipoolkrachten en de waterstofbinding tussen de watermoleculen helpen het mengsel verder te stabiliseren.
 Hoe mensen, voedsel en water de grote verspreiding van herbivoren in Oost-Afrikaanse savannes beïnvloeden
Hoe mensen, voedsel en water de grote verspreiding van herbivoren in Oost-Afrikaanse savannes beïnvloeden  Verminderde luchtvochtigheid verhoogt de dreiging van natuurbranden in het zuidwesten van de Verenigde Staten
Verminderde luchtvochtigheid verhoogt de dreiging van natuurbranden in het zuidwesten van de Verenigde Staten Wat zijn de beschrijvende actiewoorden voor bomen?
Wat zijn de beschrijvende actiewoorden voor bomen?  Hoe Bee Hives
Hoe Bee Hives Wat is het verschil tussen wespen en horzels?
Wat is het verschil tussen wespen en horzels?
Hoofdlijnen
- Grotere hersenen zorgen ervoor dat op kliffen nestelende zeemeeuwsoorten kunnen overleven en gedijen in stedelijke omgevingen
- Onderzoekers brengen het menselijk genoom in 4-D in kaart terwijl het vouwt
- Zijn honden en katten de zwakke schakel in de vogelgriepbewaking?
- De hoogste partiële zuurstofdruk in de bloedsomloop
- Hoe sociaal contact met zieke mieren hun nestgenoten beschermt
- Onderzoeken hoe totipotentie-pionierfactor Nr5a2 het genoom in zygoten activeert
- Twee van 's werelds theesoorten uitgestorven in het wild volgens nieuw rapport
- CDC, FDA en USDA beantwoorden grote vragen over de groeiende uitbraak van de vogelgriep
- Nieuw onderzoek om uit te zoeken hoe microben rijstplanten beïnvloeden
- Onderzoekers lossen een materiaalmysterie op voor elektronische apparaten van de volgende generatie

- Wetenschappers maken gigantische moleculaire kooien voor energieconversie en medicijnafgifte

- Stam gebruiken om oxynitride-eigenschappen te beheersen

- Quantum wapening:Quantum dots verbeteren de stabiliteit van perovskietkristallen die zonne-energie oogsten

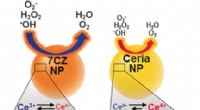
- Ceria-zirconia-nanodeeltjes als verbeterde multi-antioxidanten zijn effectief bij de behandeling van sepsis
 Interactieve kaart zal rapporten over haatmisdrijven crowdsourcen
Interactieve kaart zal rapporten over haatmisdrijven crowdsourcen Nieuwe studie daagt de populaire verklaring uit waarom een sociaal insect werker of koningin wordt
Nieuwe studie daagt de populaire verklaring uit waarom een sociaal insect werker of koningin wordt  Onderzoekers analyseren hoe 3D-geprinte metalen breken
Onderzoekers analyseren hoe 3D-geprinte metalen breken Twee NASA-satellieten om signaalverstoring vanuit de ruimte te bestuderen
Twee NASA-satellieten om signaalverstoring vanuit de ruimte te bestuderen Is vochtige lucht zwaarder dan droge lucht?
Is vochtige lucht zwaarder dan droge lucht?  Technologie die de sociale vaardigheden van kinderen tegenwoordig niet schaadt
Technologie die de sociale vaardigheden van kinderen tegenwoordig niet schaadt Tienvoudige toename van het vermogen om eiwitten in kankercellen te lokaliseren
Tienvoudige toename van het vermogen om eiwitten in kankercellen te lokaliseren Robotverzorgers kunnen eenzame senioren helpen - ze vrolijken mensen al op
Robotverzorgers kunnen eenzame senioren helpen - ze vrolijken mensen al op
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

