
Wetenschap
Wat heeft stabiliteit te maken met koolwaterstofbinding?
De stabiliteit van koolwaterstofmoleculen wordt voornamelijk bepaald door twee factoren:
1. Hefsterkte :De sterkte van de bindingen tussen koolstof- en waterstofatomen speelt een cruciale rol bij het bepalen van de stabiliteit van een koolwaterstofmolecuul. Sterkere bindingen resulteren in een stabieler molecuul. Over het algemeen zijn C-H-bindingen sterk en dragen ze aanzienlijk bij aan de stabiliteit van koolwaterstoffen.
2. Moleculaire structuur :De moleculaire structuur van een koolwaterstofmolecuul beïnvloedt ook de stabiliteit ervan. Moleculen met compactere en symmetrische structuren zijn doorgaans stabieler dan die met uitgebreide of onregelmatige structuren. Dit komt omdat compacte structuren de totale energie van het molecuul minimaliseren door de samenstellende atomen dichter bij elkaar te brengen.
Beschouw bijvoorbeeld de stabiliteit van twee structurele isomeren van hexaan:n-hexaan en 2-methylpentaan. N-hexaan heeft een lineaire structuur waarbij alle koolstofatomen in een rechte keten zijn gerangschikt. Daarentegen heeft 2-methylpentaan een vertakte structuur met een methylgroep bevestigd aan het tweede koolstofatoom van de pentaanketen.
N-hexaan is stabieler dan 2-methylpentaan omdat de lineaire structuur een betere orbitale overlap tussen de koolstof- en waterstofatomen mogelijk maakt, wat resulteert in sterkere C-H-bindingen. De vertakte structuur van 2-methylpentaan veroorzaakt enige sterische hinder, wat leidt tot iets zwakkere C-H-bindingen en verminderde algehele stabiliteit.
Bovendien kan de stabiliteit van koolwaterstofmoleculen worden beïnvloed door de aanwezigheid van extra functionele groepen of substituenten. De introductie van elektronegatieve substituenten zoals zuurstof of stikstof kan bijvoorbeeld de elektronenverdeling binnen het koolwaterstofmolecuul veranderen, waardoor de stabiliteit en reactiviteit ervan worden beïnvloed.
Het begrijpen van de stabiliteit van koolwaterstofmoleculen is essentieel op verschillende gebieden, waaronder de organische chemie, petrochemie en brandstofwetenschap. Het helpt bij het voorspellen van het gedrag en de eigenschappen van koolwaterstoffen, het ontwerpen en optimaliseren van chemische processen en het ontwikkelen van nieuwe materialen en technologieën.
 Zijn kookpunten en bevriezingsvoorbeelden van chemische eigenschappen?
Zijn kookpunten en bevriezingsvoorbeelden van chemische eigenschappen?  Waarom bevat natriumhydroxideoplossing carbonaat?
Waarom bevat natriumhydroxideoplossing carbonaat?  Een reactie waarbij licht en twee overgangsmetaalkatalysatoren worden gebruikt om anilinen te maken
Een reactie waarbij licht en twee overgangsmetaalkatalysatoren worden gebruikt om anilinen te maken Wat is een calorimeter en wat zijn de beperkingen?
Wat is een calorimeter en wat zijn de beperkingen?  Wat is het verschil tussen natriumhydroxide en kaliumhydroxide?
Wat is het verschil tussen natriumhydroxide en kaliumhydroxide?
 Groene straten:waarom het beschermen van stadsparken en struiken van cruciaal belang is naarmate onze steden dichter worden
Groene straten:waarom het beschermen van stadsparken en struiken van cruciaal belang is naarmate onze steden dichter worden  30 jaar genezing van de ozonlaag
30 jaar genezing van de ozonlaag Welke dieren hebben een Tapetum Lucidum?
Welke dieren hebben een Tapetum Lucidum?  Europees Parlement stopt met plastic waterflessen
Europees Parlement stopt met plastic waterflessen Rijke landen bereikten twee jaar te laat de doelstelling van 100 miljard dollar aan klimaatfinanciering:OESO
Rijke landen bereikten twee jaar te laat de doelstelling van 100 miljard dollar aan klimaatfinanciering:OESO
Hoofdlijnen
- Onderzoekers ontdekken hoe het Zika-virus zijn gastheercel hermodelleert om de virale productie te stimuleren
- Hoe planten suiker gebruiken om wortels te produceren
- Bewaking op afstand helpt bij het vinden van oplossingen voor crapemyrtle bark scale
- Hoe de delen van de menselijke schedel te leren
- Zaai-tussengezaaide bodembedekkers bieden voordelen voor de V3-maïsoogst
- Kan een viraal genoom worden gemaakt van zowel DNA als RNA?
- De soorten cellen die aan een membraan gebonden zijn Nucleus
- Hebben abiotische factoren invloed op biotische factoren?
- Wat betekent OD in de wetenschap?
- Onderzoek onthult nieuw mechanisme achter epilepsie en medicijnmodulatie
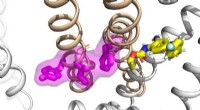
- Een uitvinding maakt de productie van een natuurlijke zoetstof mogelijk
- Vechten tegen een machtig onkruid

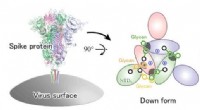
- Glycanen zijn cruciaal bij COVID-19-infectie
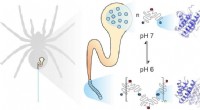
- Dynamiek van zijde-eiwitten is de sleutel tot uitstekende stabiliteit van spinzijde als biomateriaal
 Wat zijn de 3 soorten verbindingen en hun voorbeelden in de chemie?
Wat zijn de 3 soorten verbindingen en hun voorbeelden in de chemie?  Wat is de algemene vorm voor het eenvoudigste type zuur-base-reactie?
Wat is de algemene vorm voor het eenvoudigste type zuur-base-reactie?  Ierland heeft bijna al zijn inheemse bossen verloren:hier leest u hoe u ze terug kunt brengen
Ierland heeft bijna al zijn inheemse bossen verloren:hier leest u hoe u ze terug kunt brengen  George Clooney of Saddam Hoessein? Waarom betalen consumenten voor bezittingen van beroemdheden?
George Clooney of Saddam Hoessein? Waarom betalen consumenten voor bezittingen van beroemdheden?  Hoe forensische boekhouding werkt
Hoe forensische boekhouding werkt  Afstembare derde harmonische generatie in grafeen maakt de weg vrij voor snelle optische communicatie en signaalverwerking
Afstembare derde harmonische generatie in grafeen maakt de weg vrij voor snelle optische communicatie en signaalverwerking Speekseleiwitten kunnen verklaren waarom sommige mensen te veel zout gebruiken
Speekseleiwitten kunnen verklaren waarom sommige mensen te veel zout gebruiken De vier fasen van de levenscyclus van een dier
De vier fasen van de levenscyclus van een dier
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

