
Wetenschap
Wat is de molaliteit van een oplossing die wordt gemaakt door 2 mol NaOH op te lossen in 10 kg water?
Molaliteit wordt gedefinieerd als het aantal mol opgeloste stof per kilogram oplosmiddel. In dit geval is het oplosmiddel water.
Om de molaliteit te berekenen, moeten we het aantal mol NaOH en de massa van water in kilogram kennen.
De molaire massa van NaOH is 39,9971 g/mol. Dus 2 mol NaOH is 2 x 39,9971 g =79,9942 g.
De massa van water is 10 kg =10.000 g.
Daarom is de molaliteit van de oplossing:
$$Molaliteit =\frac{Moles\ van\ Opgeloste stof}{Massa\ van\ Oplosmiddel\ (in\ Kg)}$$
$$Molaliteit =\frac{2 \text{ mollen}}{10 \text{ kg}} =0,2 \text{ m}$$
 Nieuwe methode voor het identificeren van koolstofverbindingen afkomstig van fossiele brandstoffen
Nieuwe methode voor het identificeren van koolstofverbindingen afkomstig van fossiele brandstoffen Componenten van Lysis Buffers
Componenten van Lysis Buffers  Butanol in latexverf gedetecteerd door massaspectrometrietechnologie
Butanol in latexverf gedetecteerd door massaspectrometrietechnologie Wat beschrijft het beste wat er gebeurt bij een chemische reactie?
Wat beschrijft het beste wat er gebeurt bij een chemische reactie?  Welke ionen helpen de pH van speeksel te reguleren?
Welke ionen helpen de pH van speeksel te reguleren?
 Video:Aanpak van de effecten van klimaatverandering op de bessenteelt in Europa
Video:Aanpak van de effecten van klimaatverandering op de bessenteelt in Europa Omslagpunt koude regio nu onvermijdelijk
Omslagpunt koude regio nu onvermijdelijk De wederopbouw van de aardbeving in Nepal zal niet slagen totdat de kwetsbaarheid van de overlevenden is aangepakt
De wederopbouw van de aardbeving in Nepal zal niet slagen totdat de kwetsbaarheid van de overlevenden is aangepakt Opruimduiken, recycling:Libanezen reageren op afvalcrisis
Opruimduiken, recycling:Libanezen reageren op afvalcrisis Veranderingen in wind op grote hoogte boven de Stille Zuidzee produceren langetermijneffecten
Veranderingen in wind op grote hoogte boven de Stille Zuidzee produceren langetermijneffecten
Hoofdlijnen
- Hoe Shark Week liefde voor oceaanroofdieren kan inspireren
- Waarom blijft het haar op je armen kort, terwijl het hoofd erg lang kan worden?
- Onderzoek toont aan dat cabernet-druiven klimaatverandering kunnen overleven
- Onderzoek toont aan hoe genactie kan leiden tot diabetespreventie en -genezing
- Roze + roze =goud? De veren van hybride kolibries komen niet overeen met die van zijn ouders
- Veel vis in de zee? Niet noodzakelijk, zoals de geschiedenis laat zien
- Hoe reageert het immuunsysteem op veranderde zwaartekracht?
- Doodt klimaatverandering Amerikaanse zeesterren?
- Hoe gentherapie werkt
- De detectie van een date rape drug verbeteren
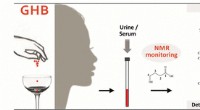
- In gloeiende kleuren:de verspreiding van medicijndeeltjes in een forensisch laboratorium zien

- Onderzoekers ontwikkelen smartphonelezer voor snellere infectietests

- Atomen herschikken in elektrolyt en regelen de ionenstroom onder zware omstandigheden
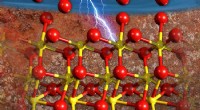
- Plastic afval omzetten in smeeroliën
 Er is een stormloop om de diepe zeebodem te ontginnen, met effecten op het leven in de oceaan die niet goed worden begrepen
Er is een stormloop om de diepe zeebodem te ontginnen, met effecten op het leven in de oceaan die niet goed worden begrepen Nanojars vangen opgeloste koolstofdioxide op, giftige ionen uit water
Nanojars vangen opgeloste koolstofdioxide op, giftige ionen uit water Wat is de vergelijking voor hydrolyse van een lipide?
Wat is de vergelijking voor hydrolyse van een lipide?  Lichaamsdelen van een krokodil
Lichaamsdelen van een krokodil  Chemicaliën die vocht absorberen
Chemicaliën die vocht absorberen Grafeen:een patroonsjabloon voor moleculaire verpakking
Grafeen:een patroonsjabloon voor moleculaire verpakking Machine learning-technologie om vreemde gebeurtenissen tussen LHC-gegevens te volgen
Machine learning-technologie om vreemde gebeurtenissen tussen LHC-gegevens te volgen Vals verhaal zegt dat archeologen Exodus-bewijs vinden
Vals verhaal zegt dat archeologen Exodus-bewijs vinden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

