
Wetenschap
Wat is de pH van een oplossing waarvan de hydroniumionconcentratie 5,03 is en nbsp acuut nbsp10-1 M?
Om de pH van een oplossing te bepalen, gebruiken we de formule:
$$pH =-\log[\text{H}_3\text{O}^+]$$
waarbij [H3O+] de hydroniumionconcentratie in mol per liter (M) voorstelt.
Gegeven de hydroniumionenconcentratie [H3O+] =5,03 × 10-10 M, kunnen we de pH als volgt berekenen:
$$pH =- \log (5,03 \maal 10^{-10})$$
$$pH =9,30$$
Daarom is de pH van de oplossing 9,30.
 Het aantal ionen in een verbinding vinden
Het aantal ionen in een verbinding vinden  Virussen onderscheiden, vernietigen E. coli in drinkwater
Virussen onderscheiden, vernietigen E. coli in drinkwater Welke voedingsmiddelen bevatten organische zuren?
Welke voedingsmiddelen bevatten organische zuren?  Welk element brandt met een blauwe vlam en geeft een zeer zuur gas af?
Welk element brandt met een blauwe vlam en geeft een zeer zuur gas af?  Nieuw onderzoek naar de risico's van blootstelling aan lood door kogels die worden gebruikt bij de jacht op groot wild
Nieuw onderzoek naar de risico's van blootstelling aan lood door kogels die worden gebruikt bij de jacht op groot wild
 Onderzoek toont de voordelen aan van het koolstofvrij maken en hernieuwbare energie voor de volksgezondheid
Onderzoek toont de voordelen aan van het koolstofvrij maken en hernieuwbare energie voor de volksgezondheid  Het verminderen van de CO2-uitstoot zal de zeespiegelstijging beperken, studie zegt:
Het verminderen van de CO2-uitstoot zal de zeespiegelstijging beperken, studie zegt: Droogte in Australië breidt zich uit ondanks wijdverbreide, aanzienlijke regen
Droogte in Australië breidt zich uit ondanks wijdverbreide, aanzienlijke regen Hoe is water een hernieuwbare hulpbron?
Hoe is water een hernieuwbare hulpbron?  Motiveert racistische wrok het vertrouwen in valse overtuigingen?
Motiveert racistische wrok het vertrouwen in valse overtuigingen?
Hoofdlijnen
- Bodembedekkers bieden een bed &breakfast-tussenstop voor trekvogels
- Nieuw onderzoek suggereert dat diverse hoofddeksels bij hoefdieren zijn geëvolueerd uit een gemeenschappelijke voorouder
- Kan synthetische biologie wilde dieren redden?
- Hoe manukahoning infecties helpt bestrijden
- Hersenen hoe je werkt
- Wat betekenen de bloedgroepletters?
- Exotische dieren en de jacht op goud
- Planten worden toleranter als ze in symbiose met schimmels leven
- Hoe goed worden alternatieve eiwitbronnen ontvangen door de eindconsument?
- Tomaten van dezelfde kwaliteit als normaal, maar met slechts de helft van het water

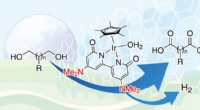
- Team synthetiseert gelijktijdig dicarbonzuren en waterstof uit diolen
- Wetenschappers ontdekken sleutelmechanisme achter de vorming van spinrag

- Hydrogel met langzame afgifte helpt immunotherapie voor kanker
- Nieuwe milieuvriendelijke synthesemethode maakt gebruik van aluminiumoxide als recyclebare katalysator

 Een nieuwe brandstofcel-elektrolyt
Een nieuwe brandstofcel-elektrolyt Ruimte, de laatste grens voor miljardair Richard Branson
Ruimte, de laatste grens voor miljardair Richard Branson Hoe jonge oesters de metamorfose van vleesetende buikpotige Rapana venosa beïnvloeden
Hoe jonge oesters de metamorfose van vleesetende buikpotige Rapana venosa beïnvloeden Je doelen bereiken:helpt het om jezelf uit het grote geheel te verwijderen?
Je doelen bereiken:helpt het om jezelf uit het grote geheel te verwijderen?  Hoe het Terracottaleger werkt
Hoe het Terracottaleger werkt  Spin-levensduur van elektronen in grafeen verhoogd door magnetische velden
Spin-levensduur van elektronen in grafeen verhoogd door magnetische velden Hoe hectes in een cirkel berekenen
Hoe hectes in een cirkel berekenen  Onderzoekers beschrijven privacygerelateerde juridische, ethische uitdagingen met satellietgegevens
Onderzoekers beschrijven privacygerelateerde juridische, ethische uitdagingen met satellietgegevens
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

