
Wetenschap
Hoe verhoudt een oplossing met een pH van 7 zich tot 5?
De pH-schaal is logaritmisch, wat betekent dat elk geheel getal verschil in pH een tienvoudig verschil in zuurgraad of basiciteit vertegenwoordigt. Een oplossing met een pH van 5 is bijvoorbeeld tien keer zuurder dan een oplossing met een pH van 6.
De pH van een oplossing wordt bepaald door de concentratie waterstofionen (H+) in de oplossing. Hoe meer waterstofionen er in een oplossing zitten, hoe zuurder deze is. Omgekeerd geldt:hoe minder waterstofionen er in een oplossing zitten, hoe basischer deze is.
De pH van een oplossing is belangrijk omdat deze de chemische reacties die in de oplossing plaatsvinden, kan beïnvloeden. Sommige enzymen werken bijvoorbeeld alleen bij een specifieke pH. Als de pH van de oplossing te hoog of te laag is, kan het enzym niet goed functioneren.
De pH van een oplossing kan ook worden gebruikt om de oplosbaarheid van stoffen in de oplossing te bepalen. Sommige stoffen zijn bijvoorbeeld beter oplosbaar in zure oplossingen, terwijl andere beter oplosbaar zijn in basische oplossingen.
De pH van een oplossing is een belangrijke factor die de chemische reacties die in de oplossing plaatsvinden en de oplosbaarheid van stoffen in de oplossing kan beïnvloeden.
 Wetenschappers vechten om uniek koraalrif in Guyana te redden
Wetenschappers vechten om uniek koraalrif in Guyana te redden Bevingen in Lake Erie veroorzaakt door veranderende waterstanden? Studie vindt geen smoking gun, dringt aan op verder onderzoek
Bevingen in Lake Erie veroorzaakt door veranderende waterstanden? Studie vindt geen smoking gun, dringt aan op verder onderzoek Onderzoekers tonen de beste methoden om de met uitsterven bedreigde specht te helpen
Onderzoekers tonen de beste methoden om de met uitsterven bedreigde specht te helpen  Koudwaterstromen kunnen een toevluchtsoord bieden tegen het veranderende klimaat
Koudwaterstromen kunnen een toevluchtsoord bieden tegen het veranderende klimaat Decennium van zware stormen heeft de gletsjers in het noordwesten geholpen, maar verwacht niet dat het zo blijft, onderzoeken tonen aan
Decennium van zware stormen heeft de gletsjers in het noordwesten geholpen, maar verwacht niet dat het zo blijft, onderzoeken tonen aan
Hoofdlijnen
- Ontdekken wat durian doet stinken
- Het symposium in Pittsburgh antwoordt:Wat is Watson?
- Hoe een RNA-gen een heel chromosoom tot zwijgen brengt
- Hoe cellen zichzelf meten
- Hoe maken planten zuurstof? Vraag het aan cyanobacteriën
- Als wetenschappers DNA kopiëren, knippen ze eerst het deel eruit. Welke moleculen gebruiken dit?
- Welke organismen gebruiken cellulaire ademhaling?
- Samen sterker:hoe eiwitfilamenten op elkaar inwerken
- Sexy of weerzinwekkend? Vlindervleugels kunnen zowel voor partners als voor roofdieren zijn
- Wetenschappers bedenken diervrije testen van dodelijke neurotoxines

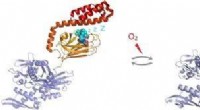
- S-glutathionylering van door mensen induceerbaar Hsp70 onthult een regulerend mechanisme met betrekking tot het C-terminale α-helix deksel
- Flow chemie techniek biedt snellere, veiligere manier om te screenen, bestuderen en optimaliseren van industriële chemische reacties

- Wat veroorzaakt het verval van oplaadbare batterijen? Hangt ervan af hoe vaak je het hebt opgeladen

- Waarom drinkwater moet worden gecontroleerd op hiv-medicijnen

 Wetenschappers vinden moleculaire vernietigingscode voor enzym dat betrokken is bij cholesterolproductie
Wetenschappers vinden moleculaire vernietigingscode voor enzym dat betrokken is bij cholesterolproductie Onderzoekers ontwikkelen duurzame nano-framboos om giftige koolmonoxide te neutraliseren
Onderzoekers ontwikkelen duurzame nano-framboos om giftige koolmonoxide te neutraliseren De elektriciteitssector in Australië moet de CO2-uitstoot tegen 2030 met 45% verminderen
De elektriciteitssector in Australië moet de CO2-uitstoot tegen 2030 met 45% verminderen Resulterende krachten berekenen
Resulterende krachten berekenen  Turbulentie ontrafelen:nieuwe inzichten in hoe vloeistoffen transformeren van orde naar wanorde
Turbulentie ontrafelen:nieuwe inzichten in hoe vloeistoffen transformeren van orde naar wanorde Metingen door scholieren hebben de weg vrijgemaakt voor belangrijke onderzoeksresultaten
Metingen door scholieren hebben de weg vrijgemaakt voor belangrijke onderzoeksresultaten Onderzoekers ontsluiten essentiële inzichten in het reactiemechanisme van metaal-stikstof-koolstof-katalysatoren
Onderzoekers ontsluiten essentiële inzichten in het reactiemechanisme van metaal-stikstof-koolstof-katalysatoren  Alle tekenen wijzen erop dat de wereld de grens van de opwarming van de aarde van 1,5 graden overschrijdt – dit is wat we er nog aan kunnen doen
Alle tekenen wijzen erop dat de wereld de grens van de opwarming van de aarde van 1,5 graden overschrijdt – dit is wat we er nog aan kunnen doen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

