
Wetenschap
Hoeveel ongedeelde elektronen en bindingen bestaan er rond het centrale atoom in ozon O3?
Om het aantal ongedeelde en bindende elektronen rond het centrale zuurstofatoom te bepalen, kunnen we de volgende stappen gebruiken:
1. Bereken het totale aantal valentie-elektronen in het molecuul: 6 (centrale zuurstof) + 6 (terminale zuurstof 1) + 6 (terminale zuurstof 2) =18 valentie-elektronen.
2. Bepaal het aantal valentie-elektronen dat wordt gebruikt bij binding: Elke zuurstof-zuurstofbinding bestaat uit twee gedeelde elektronen. Er zijn twee zuurstof-zuurstofbindingen in ozon, dus er worden in totaal vier elektronen gebruikt bij de binding.
3. Bereken het aantal niet-gedeelde elektronen: De resterende valentie-elektronen die niet bij de binding betrokken zijn, worden als ongedeelde elektronen beschouwd. In ozon zijn er 18 totale valentie-elektronen en 4 bindende elektronen, dus er zijn 18 - 4 =14 ongedeelde elektronen rond het centrale zuurstofatoom.
4. Bepaal het aantal bindende elektronen: Zoals berekend in stap 2 zijn er 4 bindende elektronen rond het centrale zuurstofatoom.
Daarom heeft het centrale zuurstofatoom in ozon 14 ongedeelde elektronen en 4 bindingselektronen.
 Welke machines worden gebruikt om katoen te oogsten?
Welke machines worden gebruikt om katoen te oogsten?  De arctische vergroening, maar het zal ons niet redden
De arctische vergroening, maar het zal ons niet redden Drie manieren waarop blockchain de wereld ertoe kan brengen op te treden tegen de klimaatcrisis
Drie manieren waarop blockchain de wereld ertoe kan brengen op te treden tegen de klimaatcrisis Suomi NPP satellietvolgsysteem tropische cycloon Cebile
Suomi NPP satellietvolgsysteem tropische cycloon Cebile Wanneer ontwikkeling en behoud botsen in de Serengeti
Wanneer ontwikkeling en behoud botsen in de Serengeti
Hoofdlijnen
- Vier nieuwe soorten slakken beschreven
- PITT-traject:Wetenschappers ontdekken hoe cellen een levensduurbevorderend 'recyclingsysteem' repareren
- Suikergom staat bekend als riskante takdruppelaars, maar is belangrijk voor bijen, papegaaien en buidelratten.
- Wat is de genetische code opgeslagen in DNA dat wordt gebruikt om eiwitproducten te produceren?
- Kunnen ziektedetecterende honden de dikhoornschapen in South Dakota helpen redden?
- Honden die als puppy gekweekt worden, vertonen slechter gedrag, lijden aan een slechte gezondheid en sterven jong – dus adopteer, ga niet winkelen
- Nieuwe technologie verlicht microben die niet in een laboratorium kunnen worden gekweekt
- Studie maakt duidelijk waarom sommige insecten hun moeders doden
- Een vogel in de bush is $223 waard, 851 in de hand
- Magnetische behandeling kan helpen bij het verwijderen van de smaak van wijnen
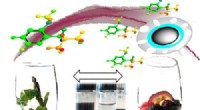
- Magneten scheiden op duurzame wijze mengsels van zeldzame aardmetalen

- Duurzame sterk geleidende elektrodematerialen van ultradunne koolstof nanovezel aerogels afgeleid van nanofibrillated
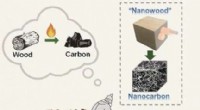
- Chemici ontdekken nieuwe reactiviteit van gespannen moleculen

- Onderzoekers stellen nieuwe strategie voor om methaanhydroxylering te verbeteren
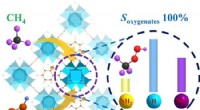
 Hoe vitaminewater werkt
Hoe vitaminewater werkt  Bewaken van genetische mutaties die belangrijk zijn voor panterbeheer in Florida
Bewaken van genetische mutaties die belangrijk zijn voor panterbeheer in Florida Hoe werkt de natriumkaliumpomp?
Hoe werkt de natriumkaliumpomp?  Een nieuw hulpmiddel voor de identificatie van niet-coderend RNA van planten
Een nieuw hulpmiddel voor de identificatie van niet-coderend RNA van planten  Inzicht in enzymevolutie baant de weg voor groene chemie
Inzicht in enzymevolutie baant de weg voor groene chemie Wat is er gebeurd in Haïti?
Wat is er gebeurd in Haïti?  Waarom zijn natrium en chloor geen stabiele elementen?
Waarom zijn natrium en chloor geen stabiele elementen?  NASA Goddard-teams om ongeopende Apollo-monsters te bestuderen
NASA Goddard-teams om ongeopende Apollo-monsters te bestuderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

