
Wetenschap
Welk subatoom bepaalt de chemische eigenschappen van het atoom en waarom?
1. Elektronenconfiguratie :De rangschikking van elektronen in de energieniveaus van een atoom, bekend als de elektronenconfiguratie, bepaalt het chemische gedrag van het atoom. De buitenste elektronen, valentie-elektronen genoemd, zijn het meest betrokken bij chemische reacties. Atomen met vergelijkbare elektronenconfiguraties hebben doorgaans vergelijkbare chemische eigenschappen.
2. Elektronegativiteit :Elektronegativiteit is het vermogen van een atoom om elektronen naar zichzelf toe te trekken. Atomen met een hoge elektronegativiteit hebben de neiging elektronen weg te trekken van andere atomen, waardoor ionische bindingen ontstaan. Atomen met een lage elektronegativiteit geven gemakkelijk hun elektronen op en vormen covalente bindingen.
3. Valentie-elektronen :Valentie-elektronen zijn de elektronen in het buitenste energieniveau van een atoom. Ze nemen deel aan chemische bindingen door overdracht (in ionische bindingen) of te delen (in covalente bindingen) met andere atomen. Het aantal valentie-elektronen bepaalt de valentie van een atoom, wat cruciaal is bij het vormen van stabiele chemische verbindingen.
4. Chemische binding :Chemische bindingen worden gevormd wanneer atomen op elkaar inwerken om een stabiele elektronenconfiguratie te bereiken. Het type chemische binding dat wordt gevormd, hangt af van de elektronenconfiguratie en de elektronegativiteit van de betrokken atomen. Covalente bindingen zijn het gevolg van het delen van elektronen, terwijl ionische bindingen voortkomen uit de volledige overdracht van elektronen.
5. Reactiviteit :De reactiviteit van een atoom wordt beïnvloed door zijn elektronenconfiguratie. Atomen met lage ionisatie-energieën (gemakkelijk verwijderbare valentie-elektronen) en hoge elektronenaffiniteiten (sterke aantrekkingskracht voor elektronen) zijn doorgaans reactiever. Deze reactiviteit bepaalt hoe een atoom interageert met andere atomen en chemische verbindingen vormt.
Samenvattend bepalen het aantal valentie-elektronen, de elektronegativiteit en de elektronenconfiguratie de chemische eigenschappen van een atoom. Deze factoren bepalen hoe atomen met elkaar omgaan en verschillende soorten chemische bindingen en verbindingen vormen. Het begrijpen van elektronengedrag en elektronenconfiguraties vormt de basis voor het voorspellen en verklaren van de chemische eigenschappen van elementen en verbindingen.
 Tip van de ijsberg:de ware staat van drinkwateradviezen in First Nations
Tip van de ijsberg:de ware staat van drinkwateradviezen in First Nations Kunstmatige intelligentie - een gamechanger voor klimaatverandering en het milieu
Kunstmatige intelligentie - een gamechanger voor klimaatverandering en het milieu Mysterieziekte verspreidt zich, bedreigt koraalriffen in Lower Florida Keys
Mysterieziekte verspreidt zich, bedreigt koraalriffen in Lower Florida Keys Wat kunnen uitgestorven soorten doen om het behoud te bevorderen?
Wat kunnen uitgestorven soorten doen om het behoud te bevorderen?  De nieuwsgierigheid van cichliden bevordert de biodiversiteit:hoe verkennend gedrag helpt bij ecologische aanpassing
De nieuwsgierigheid van cichliden bevordert de biodiversiteit:hoe verkennend gedrag helpt bij ecologische aanpassing
Hoofdlijnen
- Verkeerd gelabeld haaienvlees is wijdverbreid op de Australische markten, zo blijkt uit onderzoek
- Ze aanzetten, uitzetten – hoe je stamcellen onder controle kunt houden
- Zangvogels met unieke kleuren worden eerder als huisdier verhandeld
- Wat is lachtherapie?
- Wat is de afbraak van sucrase?
- Het risico op dementie bij honden neemt toe met elk extra levensjaar
- Wat de neus van een mot weet
- Exploderende kamikazebacteriën:hoe een paar ‘soldaatcellen’ de bevolking virulentie verlenen door zichzelf op te offeren
- Genetische technologie onthult hoe giftige paddenstoelen gifstoffen produceren
- Onderzoekers ontwikkelen duurzame methode om vanilline te winnen uit houtverwerkingsafval

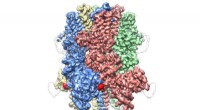
- Cryo-EM onthult kroonachtige structuur van eiwit dat verantwoordelijk is voor het reguleren van de bloedstroom
- Video:Is uw katalysator gestolen? Dit is waarom

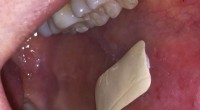
- Gips dat in de mond blijft plakken, kan de behandeling van orale aandoeningen verbeteren
- De schoonste waterdruppel ter wereld

 Precisie zeven van gassen door atomaire poriën in grafeen
Precisie zeven van gassen door atomaire poriën in grafeen Welke structuur is verantwoordelijk voor de productie van nieuwe moleculen?
Welke structuur is verantwoordelijk voor de productie van nieuwe moleculen?  Wat is het verschil tussen een bloedmaan en een maansverduistering?
Wat is het verschil tussen een bloedmaan en een maansverduistering?  Wetenschappers ontwikkelen verkeersmonitoringsysteem op basis van kunstmatige intelligentie
Wetenschappers ontwikkelen verkeersmonitoringsysteem op basis van kunstmatige intelligentie Nieuwe studie onderzoekt hoe de kosten de beslissingen om te trouwen beïnvloeden
Nieuwe studie onderzoekt hoe de kosten de beslissingen om te trouwen beïnvloeden  Cruise werkt software voor autonome voertuigen bij na crash
Cruise werkt software voor autonome voertuigen bij na crash Sniff-cam om ziekte op te sporen
Sniff-cam om ziekte op te sporen Nieuwe inzichten in de belangrijkste oorzaak van een miskraam, geboorteafwijkingen ontdekt
Nieuwe inzichten in de belangrijkste oorzaak van een miskraam, geboorteafwijkingen ontdekt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

