
Wetenschap
Hoe beïnvloedt een variabele de groei van kristallen?
1. Temperatuur:Temperatuur speelt een cruciale rol bij de kristalgroei. Hogere temperaturen verhogen over het algemeen de kinetische energie van de deeltjes, wat leidt tot snellere kristalgroei. De oplosbaarheid van de opgeloste stof (de stof die de kristallen vormt) in het oplosmiddel (de vloeistof waarin de kristallen groeien) neemt echter ook toe met de temperatuur. Dit betekent dat bij hogere temperaturen meer opgeloste moleculen opgelost blijven, wat resulteert in een langzamere kristalgroei.
2. Concentratie:De concentratie van de opgeloste stof in het oplosmiddel heeft een directe invloed op de kristalgroei. Hogere concentraties opgeloste stoffen leveren meer materiaal voor kristalvorming en leiden over het algemeen tot snellere groeisnelheden. Het bereiken van een punt van oververzadiging (waarbij het oplosmiddel niet langer alle opgeloste stof in oplossing kan houden) is echter essentieel. Als de concentratie te hoog is, wordt kiemvorming (de initiële vorming van kristalkiemen) moeilijk, wat resulteert in langzamere groei of zelfs het neerslaan van amorfe materialen.
3. Oververzadiging:Oververzadiging verwijst naar de toestand waarin het oplosmiddel meer opgeloste opgeloste stof bevat dan het bij een bepaalde temperatuur kan bevatten. Oververzadiging is een belangrijke drijvende kracht achter kristalgroei. Hoe hoger de mate van oververzadiging, hoe sneller de kristalgroeisnelheid. Overmatige oververzadiging kan echter leiden tot ongecontroleerde kiemvorming, wat resulteert in kleinere kristallen of zelfs kristalagglomeratie.
4. Onzuiverheden:Onzuiverheden in de oplossing kunnen de kristalgroei aanzienlijk beïnvloeden. Sommige onzuiverheden kunnen fungeren als kiemplaatsen, waardoor een snellere kristalgroei wordt bevorderd. Anderen kunnen de groei belemmeren door de kristalroosterstructuur te verstoren of de oppervlakte-eigenschappen van het groeiende kristal te veranderen. De aanwezigheid en concentratie van onzuiverheden kan de kristalgrootte, vorm en kwaliteit beïnvloeden.
5. pH en ionsterkte:pH en ionsterkte kunnen de oplosbaarheid en het ionisatiegedrag van de opgeloste stof beïnvloeden. Veranderingen in de pH of ionsterkte kunnen de chemische omgeving van de oplossing veranderen en de kristalgroeisnelheden en morfologieën beïnvloeden.
6. Roeren en roeren:Zacht roeren of roeren van de oplossing kan de kristalgroei bevorderen door het uniform mengen van de opgeloste stof en het oplosmiddel te bevorderen. Agitatie helpt ook de vorming van concentratiegradiënten te voorkomen en vermindert het risico op kristalclustering.
7. Toevoeging van kristalzaad:Het introduceren van kleine entkristallen in een oplossing kan dienen als kiemplaatsen en gecontroleerde kristalgroei vergemakkelijken. Deze techniek, bekend als enten, maakt de productie van kristallen met de gewenste grootte en vorm mogelijk.
Door deze variabelen te begrijpen en te beheersen, is het mogelijk het kristallisatieproces te manipuleren om kristallen te verkrijgen met specifieke eigenschappen, zoals grootte, vorm, zuiverheid en gewenste kristallografische oriëntaties, voor verschillende toepassingen in industrieën zoals de farmaceutische industrie, halfgeleiders, optica en materiaalkunde. .
 Bij EPA, coronavirus verstoort onderzoek en roept vragen op over impact op luchtkwaliteit
Bij EPA, coronavirus verstoort onderzoek en roept vragen op over impact op luchtkwaliteit Hoe spiders te identificeren met witte vlekken
Hoe spiders te identificeren met witte vlekken Hoe vertegenwoordigen wetenschappers de elementen?
Hoe vertegenwoordigen wetenschappers de elementen?  The Dangers of Rain
The Dangers of Rain  De oceaan zit vol met kleine plastic deeltjes - we hebben een manier gevonden om ze te volgen met satellieten
De oceaan zit vol met kleine plastic deeltjes - we hebben een manier gevonden om ze te volgen met satellieten
Hoofdlijnen
- Hoe vaak komt agressie bij Britse honden voor?
- Hoe nieuw bewijs van geslachtsomkeringen laat zien hoe chromosomen in de loop van de evolutionaire tijd in stand worden gehouden
- Hoe kan een fout tijdens de transcriptie het geproduceerde eiwit beïnvloeden?
- Waarom worden algoritmen algoritmen genoemd? Een korte geschiedenis van de Perzische polymath die je waarschijnlijk nog nooit hebt gehoord
- Verschillen in de hersenen kunnen verklaren waarom mannen en vrouwen pijnverlichting anders ervaren
- Welke pakketten materialen van het endoplasmatisch reticulum en verzendt ze naar andere delen van de cel?
- Wat doet een bladcel?
- Schimmelmicroben als biomeststoffen in landbouw en tuinieren:is de beloning groter dan het risico?
- Onderzoek naar acceptatie van evolutie voor beter wetenschappelijk onderwijs
- Voor ernstig zieke patiënten op life support, scheikunde kan hen helpen overleven

- Kathodedefecten verbeteren de batterijprestaties

- Afval van het maken van paarse maïschips levert een natuurlijke kleurstof op, supplementen, kattenbakvulling

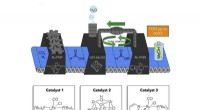
- Tandem katalytisch systeem zet koolstofdioxide efficiënt om in methanol
- De donkere materie van de moleculaire wereld identificeren

 Hoe een acre berekenen
Hoe een acre berekenen  De rol van temporele fluctuaties voor het swinggevoel in jazzmuziek
De rol van temporele fluctuaties voor het swinggevoel in jazzmuziek Je brein op Mars:hoe wetenschappers de mentale prestaties van astronauten tijdens missies volgen
Je brein op Mars:hoe wetenschappers de mentale prestaties van astronauten tijdens missies volgen Uit onderzoek blijkt hoeveel CEO's belangrijk zijn voor de prestaties van een bedrijf
Uit onderzoek blijkt hoeveel CEO's belangrijk zijn voor de prestaties van een bedrijf Eyes in the sky-project zal vervuilingen in elektriciteitscentrales vertonen
Eyes in the sky-project zal vervuilingen in elektriciteitscentrales vertonen Waarom het leveren van de nodige energie om een einde te maken aan armoede de aarde niet hoeft te kosten?
Waarom het leveren van de nodige energie om een einde te maken aan armoede de aarde niet hoeft te kosten? Aarde versus asteroïden:mensen slaan terug
Aarde versus asteroïden:mensen slaan terug Vulkanische as kan helpen bij het verminderen van koolstofdioxide in verband met klimaatverandering
Vulkanische as kan helpen bij het verminderen van koolstofdioxide in verband met klimaatverandering
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

