
Wetenschap
Hoe verschillen zuren en basen, hoe verschillen hun pH-waarden?
De pH-schaal loopt van 0 tot 14. Een pH-waarde van 7 wordt als neutraal beschouwd, pH-waarden onder de 7 duiden op een zure oplossing en pH-waarden boven de 7 duiden op een basische oplossing.
- In een zure oplossing is de concentratie H+-ionen hoger, wat aangeeft dat de oplossing meer waterstofionen en minder hydroxide-ionen (OH-) bevat
- In een basische oplossing is de concentratie H+-ionen lager, wat aangeeft dat de oplossing minder waterstofionen en meer hydroxide-ionen (OH-) bevat.
Het pH-verschil tussen zuren en basen is in essentie het verschil in waterstofionen (H+) concentratie tussen de twee oplossingen. Hoe hoger de H+ ionenconcentratie, hoe lager de pH-waarde, en hoe hoger de OH-ionenconcentratie, hoe hoger de pH-waarde.
De sterkte of intensiteit van zuren en basen houdt ook verband met hun pH-waarden. Sterke zuren of basen dissociëren volledig in water, wat resulteert in een hoge concentratie H+ ionen of OH-ionen en extreme pH-waarden. Zwakke zuren of basen dissociëren slechts gedeeltelijk in water, wat resulteert in een lagere concentratie H+ of OH-ionen en minder uitgesproken pH-waarden.
 Wat is een verbinding die hyroniumionen in water produceert?
Wat is een verbinding die hyroniumionen in water produceert?  Stikstof komt op de snelle rijstrook voor chemische synthese
Stikstof komt op de snelle rijstrook voor chemische synthese Hoe wetenschappers infectieveroorzakende biofilms bestrijden
Hoe wetenschappers infectieveroorzakende biofilms bestrijden Twee atomen van hetzelfde element wanneer ze gebonden zijn vORM A?
Twee atomen van hetzelfde element wanneer ze gebonden zijn vORM A?  Onderzoekers ontwikkelen een vast materiaal met mobiele deeltjes die reageren op de omgeving
Onderzoekers ontwikkelen een vast materiaal met mobiele deeltjes die reageren op de omgeving
 Luchtkwaliteitstests moeten worden vereenvoudigd om gevaarlijke emissies te helpen verminderen
Luchtkwaliteitstests moeten worden vereenvoudigd om gevaarlijke emissies te helpen verminderen Hoe uitputting van natuurlijke hulpbronnen te voorkomen
Hoe uitputting van natuurlijke hulpbronnen te voorkomen COVID-19 lockdown benadrukt ozonchemie in China
COVID-19 lockdown benadrukt ozonchemie in China Satellieten die een duidelijk beeld geven van broeikasgassen
Satellieten die een duidelijk beeld geven van broeikasgassen Stijgende zeespiegel creëert eerste inheemse Amerikaanse klimaatvluchtelingen
Stijgende zeespiegel creëert eerste inheemse Amerikaanse klimaatvluchtelingen
Hoofdlijnen
- Is de oorsprong van gekweekte kumquatsoorten betrokken bij kumquats uit Hong Kong? Waarschijnlijk niet
- Wat zijn interne skeletten?
- Meloensmaak gedecodeerd:de genetische sleutels tot aromatische diversiteit
- Wat wordt geoxideerd en wat wordt er gereduceerd in celademhaling?
- Productietijden kunnen het illegaal witwassen van wilde dieren tegengaan
- Hoe dicht zijn we bij het creëren van een universele bloedgroep?
- Wat is de naam van uit dierlijke polysachariden samengestelde glucose-eenheden?
- Hoe kakkerlakken hun roofdieren 'gissen'
- Kleine bijen spelen een grote rol in het geheime seksleven van bomen
- Onderzoek naar betere biotransformaties

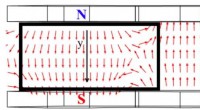
- De invloed van magnetische velden op dunnefilmstructuren
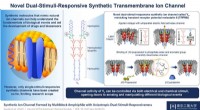
- Dubbel genot:nieuw synthetisch transmembraan-ionkanaal kan op twee manieren worden geactiveerd
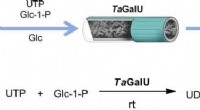
- Stap voor stap naar het eindproduct via enzymkatalyse
- Onderzoekers ontwikkelen op tillandsia geïnspireerde hygroscopische fotothermische organogels voor atmosferische waterwinning

 China's Huawei ziet winst opveren ondanks tegenslagen in de VS
China's Huawei ziet winst opveren ondanks tegenslagen in de VS Echte blauwe keuzes:een momentopname van de favoriete porno van Australië
Echte blauwe keuzes:een momentopname van de favoriete porno van Australië Webb voltooit testen en bereidt zich voor op reis naar Europa's ruimtehaven
Webb voltooit testen en bereidt zich voor op reis naar Europa's ruimtehaven Luchtvervuiling door olie- en gasproductielocaties zichtbaar vanuit de ruimte
Luchtvervuiling door olie- en gasproductielocaties zichtbaar vanuit de ruimte Hoe de rivieren in de wereld veranderen
Hoe de rivieren in de wereld veranderen Studie:ouders zijn van cruciaal belang voor de manier waarop we met stress omgaan
Studie:ouders zijn van cruciaal belang voor de manier waarop we met stress omgaan  Hoyle,
Hoyle,  Nieuw bewijs suggereert seksuele arbeidsverdeling toen de landbouw in Europa ontstond
Nieuw bewijs suggereert seksuele arbeidsverdeling toen de landbouw in Europa ontstond
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

