
Wetenschap
wat is de molariteit van H30?
Om de molariteit van hydroniumionen te berekenen, moet je de concentratie hydroniumionen in mol per liter kennen. Deze informatie wordt gewoonlijk verkregen door de pH van de oplossing te meten. De pH van een oplossing is een maatstaf voor de zuurgraad of basiciteit ervan, en is omgekeerd evenredig met de waterstofionenconcentratie. Hoe lager de pH, hoe hoger de waterstofionenconcentratie, en omgekeerd.
Zodra u de pH van de oplossing kent, kunt u de volgende formule gebruiken om de molariteit van hydroniumionen te berekenen:
```
[H3O+] =10^(-pH)
```
Als de pH van een oplossing bijvoorbeeld 3 is, kan de molariteit van hydroniumionen als volgt worden berekend:
```
[H3O+] =10^(-3) =0,001 M
```
Daarom is de molariteit van hydroniumionen in een oplossing met een pH van 3 0,001 M.
 Video:De chemie achter brokjes
Video:De chemie achter brokjes Zink reguleert de opslag en afgifte van neurotransmitters
Zink reguleert de opslag en afgifte van neurotransmitters Wereldsnelheidsrecord voor polymeersimulaties meer dan honderdvoudig verbrijzeld
Wereldsnelheidsrecord voor polymeersimulaties meer dan honderdvoudig verbrijzeld Waarom wordt ijzervijlsel in een kopersulfaatoplossing na verloop van tijd kleurloos of groen?
Waarom wordt ijzervijlsel in een kopersulfaatoplossing na verloop van tijd kleurloos of groen?  De grenzen van gasdetectietechnologie verleggen
De grenzen van gasdetectietechnologie verleggen
 Het mobiliseren van wereldwijd kapitaal in de nasleep van een ramp is essentieel voor economisch herstel
Het mobiliseren van wereldwijd kapitaal in de nasleep van een ramp is essentieel voor economisch herstel Onaanvaardbare stroomonderbrekingen getroffen terwijl het brandgevaar in Californië zich naar het zuiden verspreidt
Onaanvaardbare stroomonderbrekingen getroffen terwijl het brandgevaar in Californië zich naar het zuiden verspreidt Een plan om de oceanen van de aarde te redden
Een plan om de oceanen van de aarde te redden Captain Scotts Discovery-expeditie biedt 100 jaar later inzicht in klimaatverandering
Captain Scotts Discovery-expeditie biedt 100 jaar later inzicht in klimaatverandering Onderzoekers pleiten voor consensus in de voedselvoorzieningsketen
Onderzoekers pleiten voor consensus in de voedselvoorzieningsketen
Hoofdlijnen
- Was RNA het oorspronkelijke prebiotische molecuul?
- Slapen spinnen? Uit onderzoek blijkt dat ze net als mensen kunnen dutten
- Cameravallen en andere goedkope gegevensbronnen vormen de basis voor ecologiestudies en inspanningen voor natuurbehoud
- Stop en ga in het kaliumkanaal
- Een nieuwe aanpak om te bepalen hoe kankerverwekkende bacteriën hun doelwitten vinden
- Tropische bodems zeer gevoelig voor opwarming van de aarde, waarschuwen onderzoekers
- Onzekerheid vertroebelt VN-besprekingen over biopiraterijverdrag
- Hoe de modulaire structuur van eiwitten ervoor zorgt dat de evolutie vooruitgaat
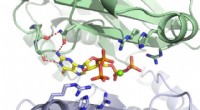
- Nieuwe analyse laat zien hoe eiwitten overgaan naar de werkmodus
- Levens-emulerende moleculen vertonen een basismetabolisme
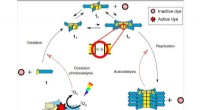
- Nieuw deactiveringsmechanisme voor gedetecteerde schakeleiwitten

- Methode om te onderzoeken hoe bacteriën reageren op honger, groei van sondecellen
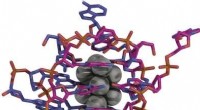
- Bepaling van de kristalstructuur van een DNA-gestabiliseerd zilveren nanocluster
- Strategische formulering van gewoon cement kan een grote impact hebben op de waterzuivering

 Onderzoek naar fruitvliegen werpt licht op hoe organismen de voedings- en vastencycli reguleren
Onderzoek naar fruitvliegen werpt licht op hoe organismen de voedings- en vastencycli reguleren  Maangrot ontdekkingsreiziger
Maangrot ontdekkingsreiziger Hoe een nieuw blauw pigment een kleurpotlood werd
Hoe een nieuw blauw pigment een kleurpotlood werd  Elcetrons die chemische bindingen vormden?
Elcetrons die chemische bindingen vormden?  Astronomen onderzoeken radioburst-emissie van de magnetar XTE J1810−197
Astronomen onderzoeken radioburst-emissie van de magnetar XTE J1810−197 NASA ontvangt wetenschappelijk rapport over het concept van de Europa-lander
NASA ontvangt wetenschappelijk rapport over het concept van de Europa-lander Waarom veranderen bladeren in de herfst van kleur?
Waarom veranderen bladeren in de herfst van kleur?  Hoe een plantfeest van een uur de geesten opheft, bouwt vaardigheden op bij vrouwen in de gevangenis
Hoe een plantfeest van een uur de geesten opheft, bouwt vaardigheden op bij vrouwen in de gevangenis
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

