
Wetenschap
Heeft NH3 een polaire binding?
De elektronegativiteit van stikstof (N) is 3,0, terwijl de elektronegativiteit van waterstof (H) 2,1 is. Dit betekent dat N een sterkere aantrekkingskracht heeft op elektronen dan H. Als gevolg hiervan wordt het elektronenpaar in de NH-binding dichter bij N getrokken, waardoor een gedeeltelijk negatieve lading op N en een gedeeltelijk positieve lading op H ontstaat. Dit resulteert in een polaire lading. band.
De polariteit van de NH-binding geeft ook aanleiding tot de algehele polariteit van het NH3-molecuul. Het stikstofatoom heeft een gedeeltelijk negatieve lading, terwijl de drie waterstofatomen een gedeeltelijk positieve lading hebben. Hierdoor ontstaat een netto positieve lading aan de waterstofzijde van het molecuul en een netto negatieve lading aan de stikstofzijde. Dit maakt NH3 een polair molecuul.
 Welk molecuul zou de laatste rustplaats kunnen worden genoemd na de gereduceerde elektronenacceptor van elektronen gedoneerd door nadh en fadh2 enz.?
Welk molecuul zou de laatste rustplaats kunnen worden genoemd na de gereduceerde elektronenacceptor van elektronen gedoneerd door nadh en fadh2 enz.?  Licht werpend op waarom kunststoffen geel worden
Licht werpend op waarom kunststoffen geel worden  Worden protonen negatief geladen deeltjes aangetroffen in de kern van een atoom?
Worden protonen negatief geladen deeltjes aangetroffen in de kern van een atoom?  Zeldzame aardmetalen worden pas waterafstotend naarmate ze ouder worden
Zeldzame aardmetalen worden pas waterafstotend naarmate ze ouder worden Is een mengsel van water en glycerol homogeen?
Is een mengsel van water en glycerol homogeen?
Hoofdlijnen
- De structuur en functie van ribosomen in eukaryoten en prokaryoten
- Wetenschappers publiceren het genoom van de waterbuffel
- Hoe recombinatie-frequenties te berekenen
- Onderzoekers ontdekken hoe overwinterende ribosomen ontwaken
- Wat is de Lewis-structuur voor HgI2?
- Hoe ureum de toegangspoort tot het leven kan zijn geweest
- De gevoeligheid van microben voor veranderingen in de omgeving hangt af van de bodemdiepte
- Voelen mannen en vrouwen pijn anders?
- Wat zijn 2 soorten permanente weefsels?
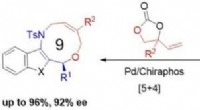
- Synthese van middelgrote ringstructuren
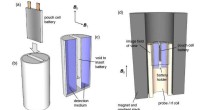
- Chemici ontwikkelen MRI-achtige techniek om te detecteren wat er aan de hand is met batterijen
- Technologie gebruikt afval van plantaardige biomassa voor zelfaangedreven biomedische apparaten

- Chemici bouwen natuurlijke antikankerverbinding met efficiënt nieuw proces

- Schoonheid in imperfectie:hoe kristaldefecten kunnen helpen afvalwarmte om te zetten in elektriciteit
 Wie domineert het discours van het verleden?
Wie domineert het discours van het verleden? Het Murdoch-imperium opbreken:wie krijgt wat?
Het Murdoch-imperium opbreken:wie krijgt wat? Lab ontwikkelt quantum dot-polymeer voor next-gen schermen
Lab ontwikkelt quantum dot-polymeer voor next-gen schermen Kummakivi, de Finse evenwichtsrots, lijkt de wetten van de natuurkunde te trotseren
Kummakivi, de Finse evenwichtsrots, lijkt de wetten van de natuurkunde te trotseren  Enorme bosbranden in het westen van de VS brengen nevel naar de oostkust
Enorme bosbranden in het westen van de VS brengen nevel naar de oostkust Onderzoekers bereiden goedkope kwantumdot-zonneverf
Onderzoekers bereiden goedkope kwantumdot-zonneverf Moeten we van de Sahara een enorme zonneboerderij maken?
Moeten we van de Sahara een enorme zonneboerderij maken? Niet-lineaire effecten in gekoppelde optische microholtes
Niet-lineaire effecten in gekoppelde optische microholtes
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

