
Wetenschap
Welke hoeveelheid zuurstof bevat hetzelfde aantal moleculen als 36 gram water?
1. Bereken het aantal moleculen in 36 gram water (H₂O):
Eerst moeten we het aantal mol water in 36 gram bepalen. De molaire massa van water (H₂O) is 18 gram per mol (2 x 1 gram voor waterstof + 16 gram voor zuurstof).
Aantal mol water (n) =massa (m) / molaire massa (M)
n =36 gram / 18 gram/mol
n =2 mol water
2. Gebruik het getal van Avogadro om het aantal moleculen te bepalen:
Het getal van Avogadro (Nₐ) is 6,022 x 10^23 moleculen per mol.
Aantal moleculen in 2 mol water =2 mol x 6,022 x 10^23 moleculen/mol
Aantal moleculen in 2 mol water =1,2044 x 10^24 moleculen
3. Bepaal de massa van zuurstof met hetzelfde aantal moleculen:
Omdat we hetzelfde aantal moleculen in zuurstof (O₂) willen, kunnen we de molaire massa van zuurstof gebruiken om de overeenkomstige massa te berekenen. De molaire massa van zuurstof (O₂) is 32 gram per mol (2 x 16 gram voor zuurstof).
Massa van zuurstof (m) =aantal moleculen (n) / Avogadro-getal (Nₐ) x molaire massa (M)
Zuurstofmassa =(1,2044 x 10^24 moleculen) / (6,022 x 10^23 moleculen/mol) x (32 gram/mol)
Massa zuurstof ≈ 6,4 gram
Daarom bevat 6,4 gram zuurstof hetzelfde aantal moleculen als 36 gram water.
 Voorbeelden van zuurbuffers
Voorbeelden van zuurbuffers  Onderzoekers vinden bewijs van eiwitvouwing op de plaats van intracellulaire druppeltjes
Onderzoekers vinden bewijs van eiwitvouwing op de plaats van intracellulaire druppeltjes Eenvoudig, goedkope methode voor het bewaken van koolstofvezel
Eenvoudig, goedkope methode voor het bewaken van koolstofvezel Robuuste en goedkope katalysatoren voor waterstofproductie
Robuuste en goedkope katalysatoren voor waterstofproductie In een ionische verbinding zijn de aantrekkingen tussen kationen en verbindingen sterker?
In een ionische verbinding zijn de aantrekkingen tussen kationen en verbindingen sterker?
Hoofdlijnen
- De uitgebreide kreten om voedsel van zangvogels vertonen de eerste tekenen van stemonderwijs
- Waarom zijn bacteriën het meest zorgwekkend?
- Wilt u voorbeelden weten van membraangebonden organellen en niet-organellen?
- Nieuwe studie over pathogene Leishmania-parasiet werpt licht op de evolutie van celkrachtproducerende machines
- Rockfish-broers en zussen werpen nieuw licht op hoe nakomelingen diffunderen en verspreiden
- AI laat zien hoe veldgewassen zich ontwikkelen:software kan toekomstige groei simuleren op basis van één enkel eerste beeld
- Landbouwproductiviteit dreef de Euro-Amerikaanse nederzetting van Utah
- Second Life-gegevens bieden inzicht in hoe trends zich verspreiden
- Een evenwicht vinden in de antibioticageneeskunde:kunnen we slechte bacteriën doden en tegelijkertijd de goede behouden?
- Nieuwe diepgaande leerbenadering voorspelt eiwitstructuur op basis van aminozuursequentie
- Lasers en vlammen:techniek kan de prestaties van hightech materialen verfijnen

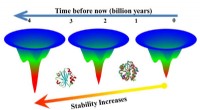
- Eiwitten die tegen de hitte kunnen
- Deuteratie van moleculen met behulp van enzymen

- Wetenschappers stellen nieuwe methode voor om atomair gedispergeerde Cu-N-C-katalysator te synthetiseren

 Babywitte haaien zijn het liefst dichter bij de kust, ontdekken wetenschappers
Babywitte haaien zijn het liefst dichter bij de kust, ontdekken wetenschappers  Eén laser is genoeg
Eén laser is genoeg Waarom je door onbeschermd eclipskijken sterren ziet
Waarom je door onbeschermd eclipskijken sterren ziet  Digitale tools voor het behoud van bosdiversiteit
Digitale tools voor het behoud van bosdiversiteit Moet ik pompoentaart in de koelkast bewaren? Voedselveiligheidsinformatie voor het seizoen
Moet ik pompoentaart in de koelkast bewaren? Voedselveiligheidsinformatie voor het seizoen  Wat is sterker ionisch of covalent?
Wat is sterker ionisch of covalent?  Om desinformatie over COVID-19 tegen te gaan, expert steunt nieuwe benadering van wetenschappelijk leren
Om desinformatie over COVID-19 tegen te gaan, expert steunt nieuwe benadering van wetenschappelijk leren Afbeelding:Italië en de Middellandse Zee
Afbeelding:Italië en de Middellandse Zee
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

