
Wetenschap
Waarom is de vergelijking onjuist Mg3 N2 Mg3N2?
De vergelijking is onjuist omdat deze in strijd is met de wet van behoud van massa. Aan de linkerkant van de vergelijking zijn er drie magnesiumatomen en twee stikstofatomen, terwijl er aan de rechterkant drie magnesiumatomen en slechts één stikstofatoom zijn. Dit betekent dat er bij de reactie één stikstofatoom verloren gaat, wat onmogelijk is.
De juiste vergelijking voor de reactie is:
$$3Mg + N_2 \rechterpijl Mg_3N_2$$
In deze vergelijking reageren drie magnesiumatomen met één stikstofmolecuul om één molecuul magnesiumnitride te produceren. Deze vergelijking behoudt massa, omdat er aan beide zijden van de vergelijking hetzelfde aantal atomen van elk element zijn.
 Is polyethyleenoxide wateroplosbaar?
Is polyethyleenoxide wateroplosbaar?  Wetenschappers ontwikkelen efficiënter katalytisch materiaal voor brandstofceltoepassingen
Wetenschappers ontwikkelen efficiënter katalytisch materiaal voor brandstofceltoepassingen Waarom wordt ijzervijlsel in een kopersulfaatoplossing na verloop van tijd kleurloos of groen?
Waarom wordt ijzervijlsel in een kopersulfaatoplossing na verloop van tijd kleurloos of groen?  Wat is de chemische samenstelling van krijt?
Wat is de chemische samenstelling van krijt?  Techniek onthult hoe kristallen zich vormen op oppervlakken
Techniek onthult hoe kristallen zich vormen op oppervlakken
 Lijst van dieren die hun eigen licht afgeven
Lijst van dieren die hun eigen licht afgeven Afbeelding:Washington D.C. vanuit een baan om de aarde
Afbeelding:Washington D.C. vanuit een baan om de aarde Monstercycloon Harold raast door Fiji (update)
Monstercycloon Harold raast door Fiji (update) Het simuleren van ballonvaren in een boorgat helpt bij het veilig boren van diepwaterolie, gas-
Het simuleren van ballonvaren in een boorgat helpt bij het veilig boren van diepwaterolie, gas- Wat is de ecologische voetafdruk van het bezitten van vis als huisdier? Een deskundige legt het uit
Wat is de ecologische voetafdruk van het bezitten van vis als huisdier? Een deskundige legt het uit
Hoofdlijnen
- Wat gebeurt er met een Zygote na bevruchting?
- Wat zijn drie fysieke eigenschappen van een banaan?
- Er worden meer koeien getest en gevolgd op vogelgriep. Dit is wat dat betekent
- Bewijs dat mensen de wereld opnieuw hebben vormgegeven? Kippen
- Wetenschappers onthullen waarom buikwantsen zo goed door je darmen kunnen zwemmen
- Hoe heet het proces waarbij delingscellen haploïde cellen vormen?
- Wat zit er aan de linkerkant van je lichaam in de menselijke anatomie?
- Herstel van de Braziliaanse Spixs-ara, gepopulariseerd in geanimeerde Rio-films, bedreigd door klimaatverandering
- Afrikaanse slaapziekte:hoe de ziekteverwekker tseetseevliegen koloniseert
- Lab-on-paper strook:Klein, goedkoop platform voor het diagnosticeren van tropische koortsen

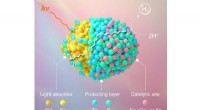
- Groeiende actieve sites op kwantumdots voor robuuste waterstoffotogeneratie
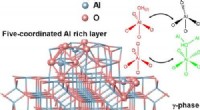
- Aard van vijf-gecoördineerd aluminium op γ-Al2O3-oppervlak
- Chemische katalysator verandert afval in schat, inerte C-H-bindingen reactief maken

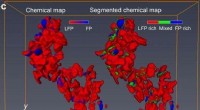
- Chemische reacties op nanoschaal in batterijen in 3D in kaart brengen
 Wetenschapsupdate over klimaatverandering:van kwaad tot erger
Wetenschapsupdate over klimaatverandering:van kwaad tot erger Een stap dichter bij het oplossen van het methaanmysterie op Mars
Een stap dichter bij het oplossen van het methaanmysterie op Mars Opgelost oplosmiddel vergelijken en contrasteren?
Opgelost oplosmiddel vergelijken en contrasteren?  Hoe zijn fytoplankton reproductie?
Hoe zijn fytoplankton reproductie?  Bolvormige sterrenhoop van de Melkweg in detail bestudeerd
Bolvormige sterrenhoop van de Melkweg in detail bestudeerd Nanobuisjes openen nieuwe weg naar kwantuminformatietechnologieën
Nanobuisjes openen nieuwe weg naar kwantuminformatietechnologieën Hoe helikopters werken
Hoe helikopters werken  Hoe groot is het acetonmolecuul?
Hoe groot is het acetonmolecuul?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

