
Wetenschap
Is sio2 zuurder dan so2?
SiO2 is zuur omdat het met water kan reageren en kiezelzuur (H4SiO4) vormt. De reactie tussen SiO2 en water kan als volgt worden weergegeven:
SiO2(s) + 2H2O(l) → H4SiO4(aq)
Bij deze reactie doneert SiO2 twee protonen aan watermoleculen, waarbij kiezelzuur- en hydroniumionen (H3O+) worden gevormd. De hydroniumionen zijn verantwoordelijk voor de zure eigenschappen van kiezelzuur.
Aan de andere kant is SO2 ook zuur, maar minder zuur dan SiO2. Dit komt omdat SO2 slechts één zuur waterstofatoom heeft, terwijl SiO2 er vier heeft. De reactie tussen SO2 en water kan als volgt worden weergegeven:
SO2(g) + H2O(l) → H2SO3(aq)
Bij deze reactie doneert SO2 één proton aan een watermolecuul, waarbij zwavelzuur (H2SO3) en hydroniumionen worden gevormd. De hydroniumionen zijn verantwoordelijk voor de zure eigenschappen van zwavelig zuur.
Omdat SiO2 meer protonen kan doneren dan SO2, is het zuurder dan SO2.
 Speciaal tijdschriftnummer zoekt naar nieuwe aanwijzingen over het oude leven
Speciaal tijdschriftnummer zoekt naar nieuwe aanwijzingen over het oude leven Gewasverzekering is goed voor boeren, maar niet altijd voor het milieu
Gewasverzekering is goed voor boeren, maar niet altijd voor het milieu Lichaamsdelen van een krokodil
Lichaamsdelen van een krokodil  Wetenschappers ontwikkelen nieuwe benadering om enorme vulkaanuitbarstingen te begrijpen
Wetenschappers ontwikkelen nieuwe benadering om enorme vulkaanuitbarstingen te begrijpen Grote tsunami trof Zuid-China in 1076, zeggen wetenschappers
Grote tsunami trof Zuid-China in 1076, zeggen wetenschappers
Hoofdlijnen
- CRISPR belooft antimicrobiële resistentie aan te pakken, maar bacteriën kunnen terugvechten
- Voors en tegens van Recombinant DNA Technology
- Hoe een parasitaire schimmel het zenuwstelsel van vliegen kaapt
- Waarom is de trekduif uitgestorven?
- Hoe groot is de kans dat Engelse leerlingen de middelbare school voltooien? Uit onderzoek blijkt dat dit afhangt van ras, geslacht en inkomen
- Hoe smaakcellen de foerageerstrategie van een heel dier kunnen controleren
- 520 miljoen jaar oud wormfossiel lost het mysterie op van hoe moderne insecten, spinnen en krabben zijn geëvolueerd
- Hoe vissen tegelijkertijd geluiden horen en maken
- Onderzoek bevestigt dat identiteitsverwisseling kan verklaren waarom haaien mensen bijten
- Nieuwe bevindingen over de recyclingcentra van cellen

- Studie onthult de rol van platina bij de conversie van schone brandstof
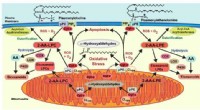
- Wat gebeurt er met plasmalogenen, de fosfolipiden waar niemand graag aan denkt
- Een biobrandstof voor geautomatiseerde warmteopwekking

- Eenvoudige methode voorgesteld voor microfabricage op niet-vlakke substraten

 Doen zonder donkere energie:wiskundigen stellen alternatieve verklaring voor kosmische versnelling voor
Doen zonder donkere energie:wiskundigen stellen alternatieve verklaring voor kosmische versnelling voor Wat maakt magneten afweren?
Wat maakt magneten afweren?  Als de dennen verdwijnen, kan het dan nog steeds Big Pine Key heten?
Als de dennen verdwijnen, kan het dan nog steeds Big Pine Key heten?  Was de Cullinan Diamond een koninklijk geschenk of een gestolen edelsteen?
Was de Cullinan Diamond een koninklijk geschenk of een gestolen edelsteen? Warmte, geen droogte, zal leiden tot lagere gewasopbrengsten, onderzoekers zeggen:
Warmte, geen droogte, zal leiden tot lagere gewasopbrengsten, onderzoekers zeggen: Nieuw model beschrijft golfgedrag in zeestraten, voorspelt moordende golven
Nieuw model beschrijft golfgedrag in zeestraten, voorspelt moordende golven Enzym ontdekt in de darm kan leiden tot nieuwe biomarker voor ziekten
Enzym ontdekt in de darm kan leiden tot nieuwe biomarker voor ziekten NASA bestelt extra astronautentaxivluchten van Boeing en SpaceX naar het ISS
NASA bestelt extra astronautentaxivluchten van Boeing en SpaceX naar het ISS
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

