
Wetenschap
Wat is hydroxide?
Hydroxide is een sterke base en een krachtig oxidatiemiddel. Het is bijtend voor metalen en kan brandwonden aan de huid en het weefsel veroorzaken. Hydroxide wordt aangetroffen in veel huishoudelijke schoonmaakmiddelen, zoals afvoerreinigers en ovenreinigers. Het wordt ook gebruikt bij de productie van papier, textiel en farmaceutische producten.
In water zijn hydroxide-ionen in evenwicht met waterstofionen, volgens de volgende vergelijking:
H2O ⇌ OH- + H+
De evenwichtsconstante voor deze reactie wordt de ionisatieconstante van water genoemd , en heeft een waarde van 1,0 × 10^-14 bij 25 °C. Dit betekent dat de concentratie hydroxide-ionen in zuiver water erg laag is, maar toeneemt naarmate de temperatuur stijgt.
De concentratie hydroxide-ionen in een oplossing kan worden gemeten met een pH-meter . De pH van een oplossing is een maatstaf voor de zuurgraad of basiciteit ervan, en wordt bepaald door de concentratie waterstofionen. Een oplossing met een pH van 7 is neutraal, een oplossing met een pH lager dan 7 is zuur en een oplossing met een pH hoger dan 7 is basisch.
Hydroxide-ionen zijn belangrijk in veel biologische processen. Ze zijn betrokken bij de regulering van de pH, het transport van voedingsstoffen en de synthese van eiwitten. Hydroxide-ionen zijn ook essentieel voor de activiteit van veel enzymen.
Hoofdlijnen
- Twee nieuwe soorten schaaldieren ontdekt op Galicische zeebodem
- Nieuwe studie vindt dat mycobacteriën de aanwezigheid van eiwitten kunnen detecteren die ziekten veroorzaken
- Drummen bij spechten lijkt neurologisch op zingen bij zangvogels
- Studie van keverflagellum biedt mogelijke manier om medische hulpmiddelen te verbeteren
- Wat zijn twee dingen die fotosynthese oplevert?
- Wat is zelfrespect?
- Faseovergang kan verklaren hoe hersenneuronen informatie coderen
- Onderzoek naar fruitvliegen werpt licht op hoe organismen de voedings- en vastencycli reguleren
- Hoe je hersenen werken
- Nieuwe strategie verbetert de selectiviteit van aromaten bij methaanomzetting

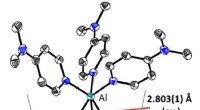
- Belangrijke mijlpaal op weg naar overgangsmetaalkatalyse met aluminium
- Review benadrukt de kracht van eenvoudige fysieke modellen voor complexe eiwitmachines

- Gericht op verborgen zak voor behandeling van beroerte en epileptische aanvallen
- Koud weken verlaagt het risico op salmonellagroei op gekiemd voedsel

 Historische klimaatschommelingen in Centraal-Europa overschat door analyse van jaarringen
Historische klimaatschommelingen in Centraal-Europa overschat door analyse van jaarringen Omgaan met stressvolle organisatieveranderingen
Omgaan met stressvolle organisatieveranderingen Staan tech-titanen op de markt?
Staan tech-titanen op de markt? Waarom heeft zwavel een grotere atoomstraal dan zuurstof?
Waarom heeft zwavel een grotere atoomstraal dan zuurstof?  Kleine vogels beschikken over een scala aan vliegstijlen dankzij hun evolutionaire voorsprong
Kleine vogels beschikken over een scala aan vliegstijlen dankzij hun evolutionaire voorsprong  Hoe luchthavenbeveiliging werkt
Hoe luchthavenbeveiliging werkt  Hoeveel water is er op aarde?
Hoeveel water is er op aarde?  Wat betekent smartphoneoorlog voor innovatie?
Wat betekent smartphoneoorlog voor innovatie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


