
Wetenschap
Welke aantrekkingskrachten houden methaanmoleculen bij elkaar?
Van der Waals-troepen
Methaan is een niet-polair molecuul en heeft dus geen permanente dipool-dipoolaantrekkingskracht. De elektronen in de methaanmoleculen zijn echter voortdurend in beweging, waardoor tijdelijke dipolen ontstaan. Deze tijdelijke dipolen kunnen dipolen induceren in aangrenzende moleculen, wat resulteert in van der Waals-krachten. De Van der Waals-krachten zijn relatief zwak, maar het zijn de enige aantrekkingskrachten tussen methaanmoleculen.
 Wat warmte ons kan vertellen over de chemie van batterijen:het Peltier-effect gebruiken om lithium-ioncellen te bestuderen
Wat warmte ons kan vertellen over de chemie van batterijen:het Peltier-effect gebruiken om lithium-ioncellen te bestuderen  Wat is materiaalstudie?
Wat is materiaalstudie?  Wat is het verschil in graad tussen Celsius versus Fahrenheit?
Wat is het verschil in graad tussen Celsius versus Fahrenheit?  Penny Science Fair Project Ideas
Penny Science Fair Project Ideas Hoe verhoudt de kern van een koperatoom zich tot een nikkelatoom?
Hoe verhoudt de kern van een koperatoom zich tot een nikkelatoom?
 Onderzoek richt zich op PFOA-bedreiging voor drinkwater
Onderzoek richt zich op PFOA-bedreiging voor drinkwater Leven op een luchtloze aarde
Leven op een luchtloze aarde Ontwikkelingsdilemma terwijl Oost-Groenland het toerisme stimuleert
Ontwikkelingsdilemma terwijl Oost-Groenland het toerisme stimuleert Klimaatrecords worden steeds weer verbroken. Dit is wat u moet weten
Klimaatrecords worden steeds weer verbroken. Dit is wat u moet weten  Online app om te visualiseren, interpretatie van ruimtelijke gegevens voor bosplanning en -behoud
Online app om te visualiseren, interpretatie van ruimtelijke gegevens voor bosplanning en -behoud
Hoofdlijnen
- Onderzoek toont aan hoe voeding de eeuwenoude hond heeft getransformeerd in een huisdier
- Wat is een CFU in de microbiologie?
- Acht nieuwe soorten kleine gekko's tuimelen uit de regenwouden van Madagaskar
- Hoe sperma het genoom van vader uitpakt, zodat het kan samensmelten met dat van moeder
- RNA's verborgen potentieel:nieuwe studie onthult zijn rol in het vroege leven en toekomstige bio-engineering
- Hoe leden van het microbioom specifiek Salmonella-infecties bestrijden
- Eén enkele haar laat onderzoekers zien wat een beer heeft gegeten
- Hoe is het complexe leven geëvolueerd? Het antwoord zou binnenstebuiten kunnen liggen
- UW-wetenschappers ontrafelen het mysterie van hoe griepvirussen zich vermenigvuldigen
- Wetenschappers gebruiken coöperatieve actie van een ligand-tegenionsysteem voor duurzame etherproductie

- Schimmelinfectie van het hoornvlies behandelen met synthetische moleculen

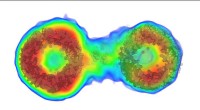
- Krachtige nieuwe beeldvormingsmethode onthult in detail hoe deeltjes in oplossing bewegen
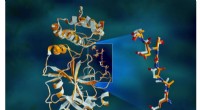
- Röntgenstralen vergroten de eiwitstructuur in het hart van het COVID-19-virus
- Onderzoekers voltooien fase één menselijke proeven met slimme pillen

 Onderzoekers bouwen een biomimetisch 'zacht kanon' om te begrijpen hoe schimmelsporen worden verspreid
Onderzoekers bouwen een biomimetisch 'zacht kanon' om te begrijpen hoe schimmelsporen worden verspreid  Turbulentie zorgt voor ijs in de wolken
Turbulentie zorgt voor ijs in de wolken Een olievlek opruimen
Een olievlek opruimen Hebben mannen en vrouwen verschillende hersenen?
Hebben mannen en vrouwen verschillende hersenen?  Koolstofsatelliet als belangrijk hulpmiddel voor politici en experts op het gebied van klimaatverandering
Koolstofsatelliet als belangrijk hulpmiddel voor politici en experts op het gebied van klimaatverandering Gletsjerfoto's illustreren klimaatverandering
Gletsjerfoto's illustreren klimaatverandering Hoe schrijf je de chemische formules van verbindingen met polyatomaire ionen?
Hoe schrijf je de chemische formules van verbindingen met polyatomaire ionen?  Online rijcursus levert real-life veiligheidsresultaten op
Online rijcursus levert real-life veiligheidsresultaten op
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

